
2019年,美国Steven Henikoff实验室成功研发CUT&Tag技术。作为全基因组水平的DNA-蛋白质互作研究方法,CUT&Tag的技术核心是运用连接有刀豆蛋白的磁珠结合细胞膜或细胞核,通过抗体将Protein A/G-Tn5转座酶融合蛋白靶向带到目标蛋白附近进行染色质切割。
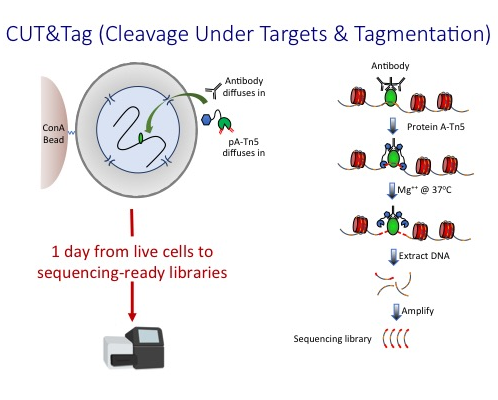
CUT&Tag的实验时间短,实验过程未对细胞核和染色质进行物理性的破坏,整个操作过程相当“温和”。因此CUT&Tag的背景噪音数据非常少,信噪比高,对起始细胞量的要求大幅减少,操作简单且数据可重复性好,更加专注于活跃的染色质位点和转录因子结合位点,备受表观遗传领域研究者的关注。目前已广泛应用于动植物的基础机制研究,并在逐步拓展至农业和医学转化。
对于起始细胞量的要求,CUT&Tag自带“低起始量光环”,研发者指出针对组蛋白,可低至100个细胞;针对转录因子,可低至1000个细胞,并且数据质量都很好,不同细胞起始量的结果也较稳定。
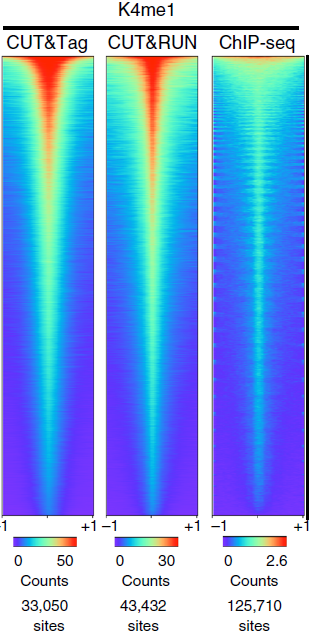
CUT&Tag的富集效果更好
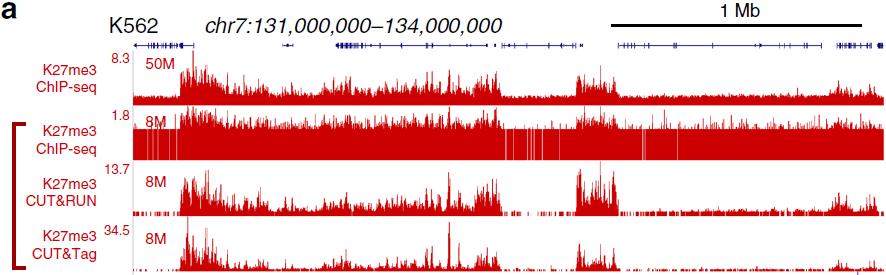
CUT&Tag的背景噪音更低
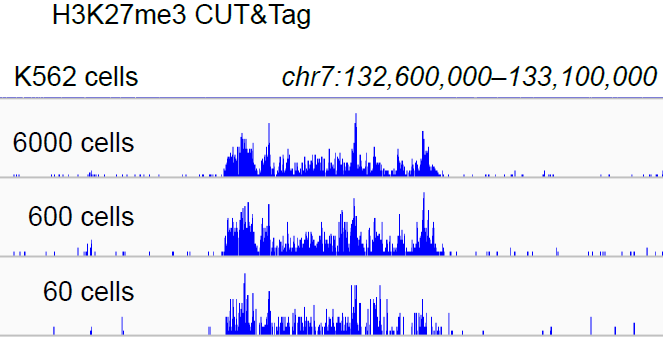
可重复性好
应用方向
(1)确定基因组上组蛋白修饰出现的位置;
(2)确定蛋白质复合体及其它反式因子在基因组上结合位点的精确定位;
(3)确定CTCF结构蛋白、转录因子和其他染色质相关蛋白如何影响表型;
(4)联合Hi-C/ATAC-seq/RNA-seq多组学数据,揭示增强子-启动子互作调控基因表达的机制。
技术路线
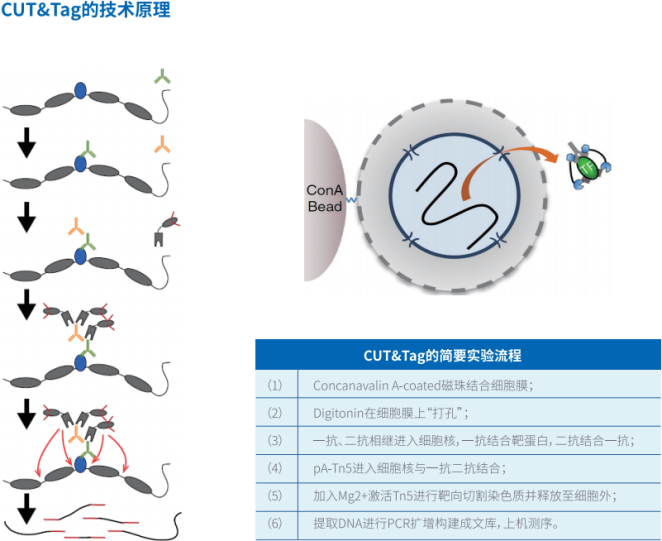
实验流程
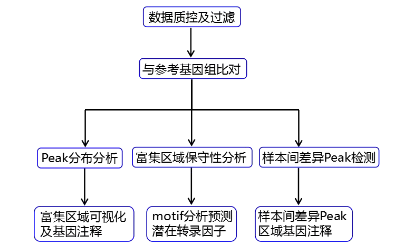
分析流程
产品参数

 微信公众号
微信公众号
