
近期,中山大学肿瘤防治中心贾卫华教授团队于人类遗传学领域的知名期刊The American Journal of Human Genetics发表题为“High-throughput identification of regulatory elements and functional assays to uncover susceptibility genes for nasopharyngeal carcinoma”的研究成果。该研究首先通过全基因组关联分析发现了两个新的鼻咽癌易感区域,9q22.33和17q12,以及两个已知的易感区域,5p15.33和9p21.3,并且通过分析这些区域的染色质开放性、组蛋白修饰和染色质互作情况,发现了一些功能性SNP和目标基因。随后,该研究通过双荧光素酶实验和CRISPRi实验验证了功能性SNP对目标基因表达的影响,确认了两个易感基因,PHF2和CDKN2B-AS1。最后,通过细胞增殖和克隆形成实验探索易感基因在NPC发生中的作用,该研究发现PHF2是一个NPC肿瘤抑制基因,而CDKN2B-AS1是一个致癌基因。永利集团3044承担了该研究中的Promoter Capture Hi-C相关工作。

图1.文章信息
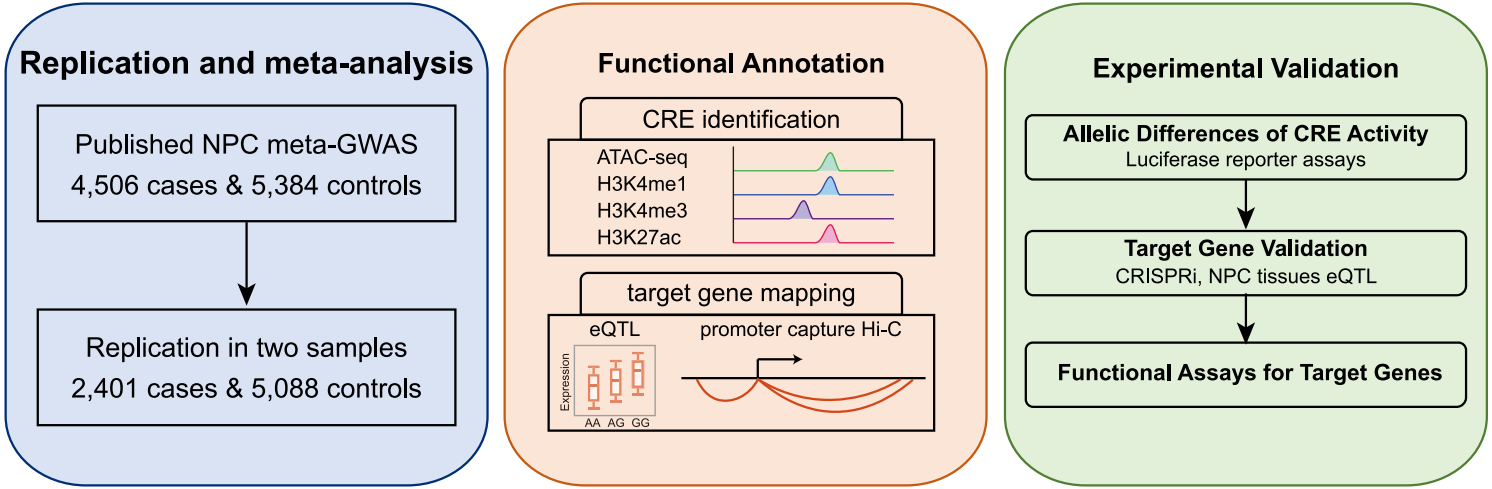
研究思路
研究材料:鼻咽癌组织、外周血,鼻咽癌细胞系(C666-1、HK1 EBV+和HK1)和鼻咽上皮细胞系(NP69)
组学方法:GWAS、ATAC-seq、ChIP-seq、Promoter Capture Hi-C(PCHi-C)、RNA-seq
验证实验:双荧光素酶实验、CRISPRi、eQTL、目的基因过表达和干扰、细胞增殖和克隆形成实验、RT-qPCR、WB
研究结果
1.Meta分析识别两个新的NPC易感位点
该研究团队早前基于四组样本(EPI-NPC-2005、NPCGEE、SYSUNPC和Hong Kong,4506例NPC病例和5384例对照)进行GWAS,发现了两个非人类白细胞抗原(HLA ) 区域——9p21.3(邻近基因:CDKN2B-AS1)和5p15.33(邻近基因:CLPTM1L/TERT)与NPC风险显著相关。在本次研究中,该团队新增两组来自中国广西和江苏的样本(2401例NPC病例和5088例对照),通过对共计六组样本进行Meta分析,鉴定了两个区域中的SNP达到全基因组显著水平,分别是9q22.33区域的rs1867277(邻近基因:FOXE1)和17q12区域的rs226241(邻近基因:LASP1/RPL23)。
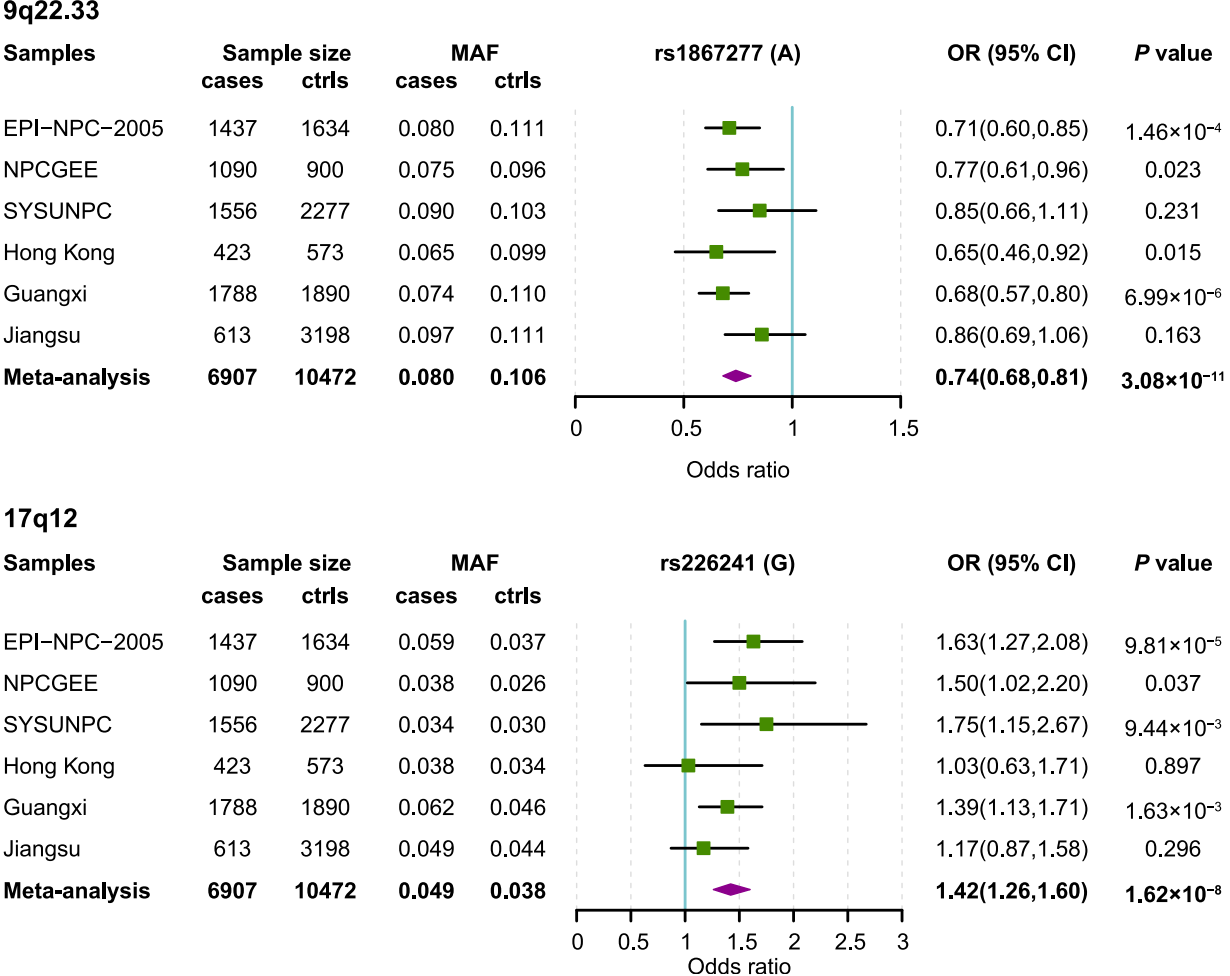
图2.两个新的NPC易感位点
2.NPC易感位点的综合功能分析
结合已有GWAS研究和上述结果,研究人员重点关注四个NPC易感位点(9q22.33、17q12、9p21.3和5p15.33)。该研究通过联合三个鼻咽癌细胞系(C666-1、HK1 EBV+和HK1)和一个鼻咽上皮细胞系(NP69)的ATAC-seq和ChIP-seq实验结果,以及C666-1细胞系的PCHi-C实验结果以分析顺式调控元件(CRE)并对这些易感位点进行注释。结果显示,CRE区域中有14个候选的功能SNP与NPC易感性关联。
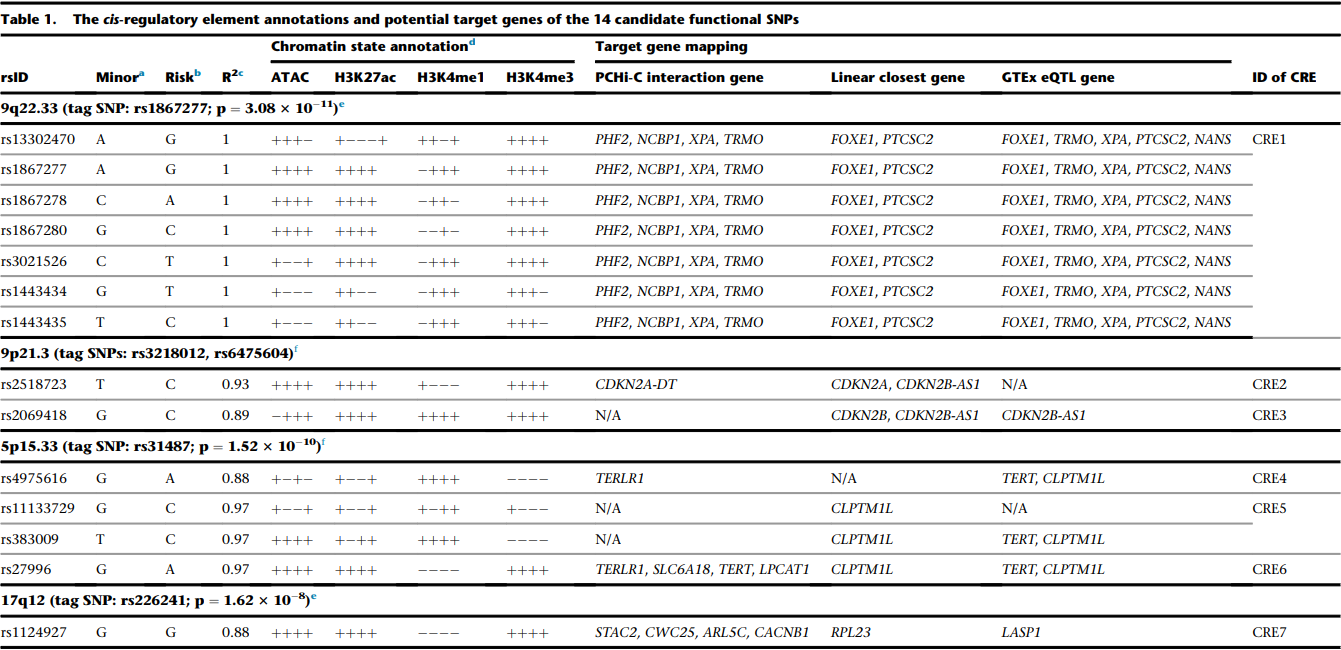
图3.CRE区域中有14个候选的功能SNP及其目标基因
随后,基于三种方法识别这些SNP的目标基因,包括分析PCHi-C数据得到与其在空间互作的基因、分析其线性相距最近的基因,以及分析GTEx数据得到其eQTL基因。其中17q12没有任何达到1.0 ×10−6显著水平的功能性SNP,5p15.33区域的一些候选的功能性SNP,如rs11133729和rs383009,位于重复序列中,因此后续重点关注的是9q22.33和9p21.3两个区域的功能性SNP及其目标基因。
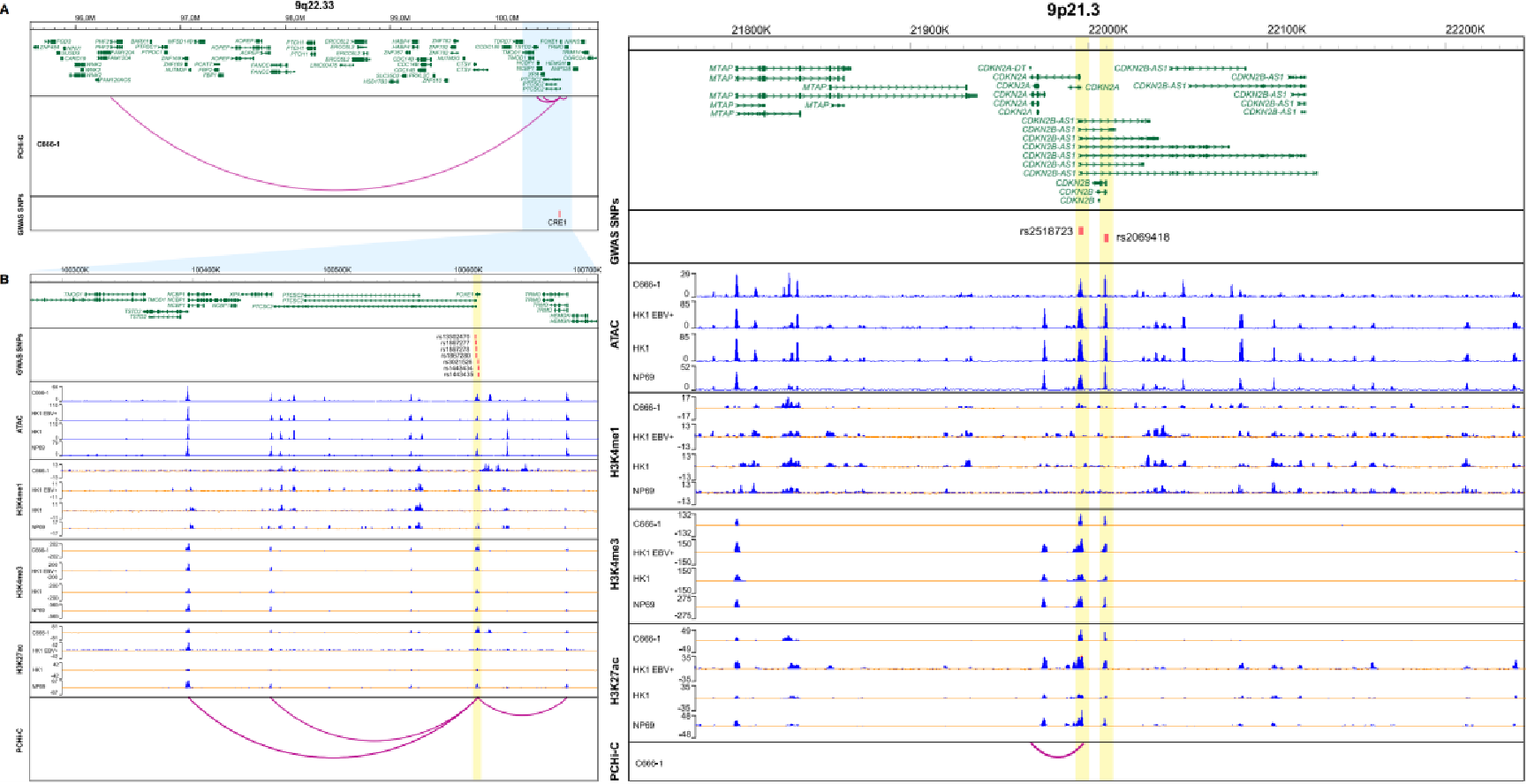
图4.9q22.33区域七个SNP(左)和9p21.3区域两个SNP(右)的功能注释
3.多实验验证9q22.33和9p21.3的功能性SNP
进一步探索9q22.33区域和9p21.3区域的候选SNP的功能作用。首先,用双荧光素酶实验在两种NPC细胞系中评估功能SNP的等位基因特异性效应,结果显示,在9q22.33区域,CRE1内的五个SNP的风险等位基因都降低了报告基因的增强子活性,而且这五个SNP之间完全连锁不平衡,形成了一个风险单倍型;在9p21.3区域,与保护性等位基因G相比,rs2069418的风险等位基因C提高了CRE3的增强子活性。然后,在两种NPC细胞系用CRISPRi技术沉默CRE1和CRE3分别使PHF2和CDKN2B-AS1的表达受到了显著抑制。
接下来,用鼻咽癌组织样本进行eQTL分析,研究发现,在9q22.33区域,CRE1中代表性SNP rs1867277的基因型与PHF2的表达水平有关联,PHF2在风险基因型(GG)样本的表达比AG基因型样本更低;在9p21.3区域,CRE3中功能SNP rs2069418的基因型与CDKN2B-AS1表达有关,CDKN2B-AS1在NPC风险基因型(CC)样本的表达高于具有杂合基因型(GC)的。
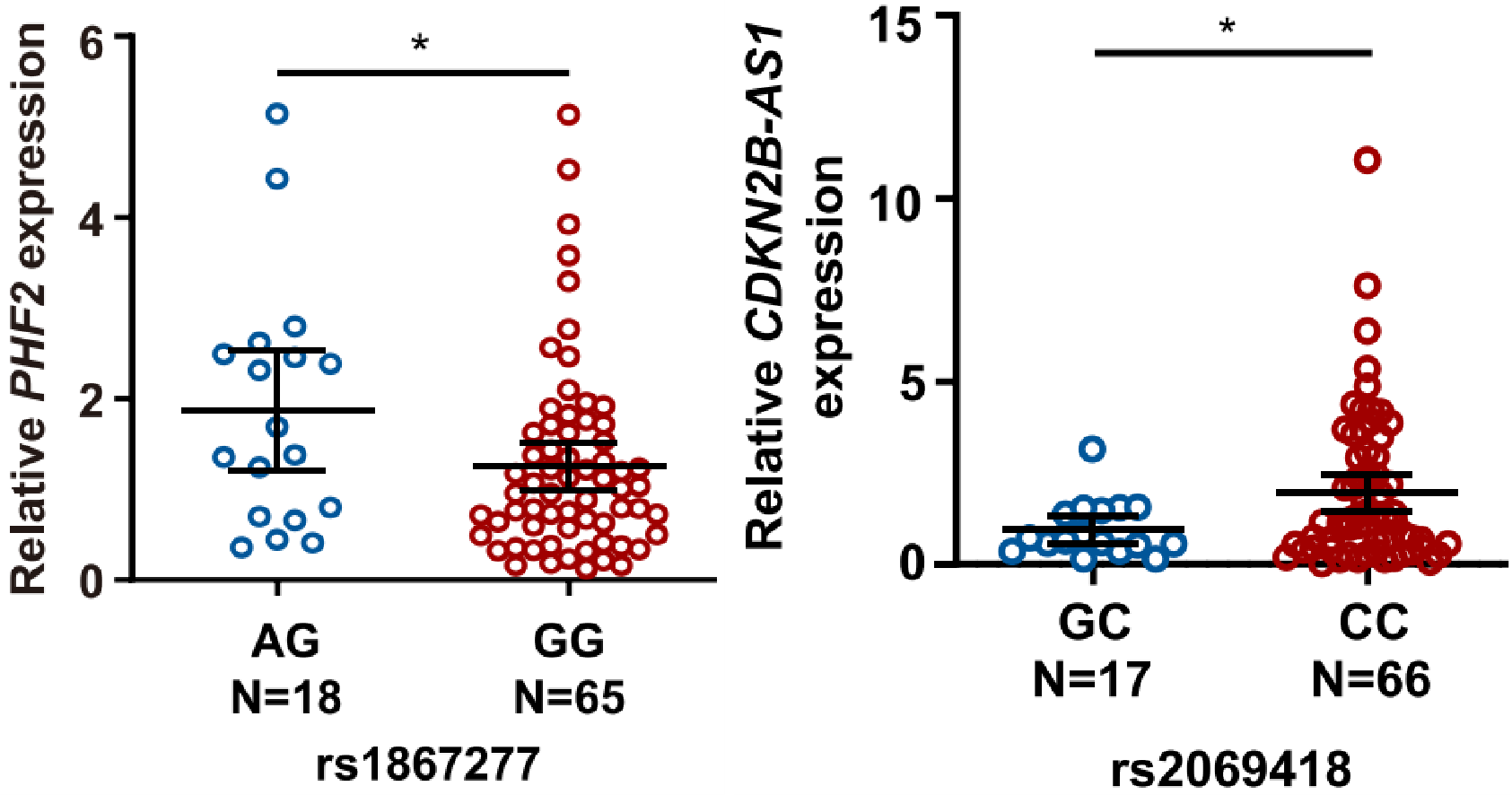
图5.PHF2在rs1867277(GG)的表达更低(左),CDKN2B-AS1在rs2069418(CC)的表达更高(右)
最后,在两种NPC细胞系中过表达或敲除PHF2/CDKN2B-AS1,研究发现,PHF2的过表达能够抑制细胞增殖和克隆形成,沉默则促进细胞增殖和克隆形成;CDKN2B-AS1的过表达促进细胞增殖和克隆形成,沉默则抑制细胞增殖和克隆形成。
因此,9q22.33区域的风险单倍型可能通过抑制CRE1的增强子活性,降低PHF2的表达水平,而PHF2可能是一个肿瘤抑制基因,它的下调有利于鼻咽癌的发展。9p21.3区域的风险SNP可能通过促进CRE3的增强子活性,增加CDKN2B-AS1的表达水平。CDKN2B-AS1可能是一个致癌基因,在鼻咽癌的发展中起到促进作用。
小 结
该研究通过GWAS和PCHi-C等方法,发现了两个新的NPC易感区域,9q22.33和17q12,以及两个已知的易感区域,5p15.33和9p21.3,并对这些区域进行了功能注释。随后,该研究通过双荧光素酶实验和CRISPRi实验,鉴定了9q22.33区域的易感基因PHF2,它是一种组蛋白去甲基化酶,具有肿瘤抑制作用。功能性SNP的风险等位基因通过抑制其远端(4.3 Mb)顺式调控元件的增强子活性,降低了PHF2的表达水平,从而促进了NPC细胞的增殖。此外,研究还发现了9p21.3区域的易感基因CDKN2B-AS1,功能性SNP的风险等位基因通过增加其增强子活性,促进了CDKN2B-AS1的表达。CDKN2B-AS1的过表达也促进了NPC细胞的增殖。总之,该研究发现了功能性SNP和NPC易感基因,为解释GWAS信号提供了新的线索和研究思路,并有助于揭示NPC发生的遗传机制。
中山大学肿瘤防治中心贾卫华教授为该论文通讯作者,中山大学肿瘤防治中心王曈旻博士和肖若雯博士为该论文共同第一作者。
该研究得到国家重点研究开发项目(2021YFC2500400)、广东省基础与应用基础研究基金(2021B1515420007)、国家重点研究开发项目(2020YFC1316902)、国家自然科学基金(82003520、82273705、81973131和81903395)和广东省基础与应用基础研究国立卫生研究院(R01CA11587301)资助。
参考文献:
Wang T M, Xiao R W, He Y Q, et al. High-throughput identification of regulatory elements and functional assays to uncover susceptibility genes for nasopharyngeal carcinoma[J]. The American Journal of Human Genetics, 2023.
 微信公众号
微信公众号
