

小时候大家应该都听过画蛇添足的故事:楚国有个权贵,拿出一壶酒赏给门人们喝。门客们互相商量说:“我们各自在地上比赛画蛇,先画好的人就喝这壶酒。” 有一个人先把蛇画好了,他拿起酒壶正要喝,却左手拿着酒壶,右手继续画蛇,说:“我能够给它画脚。”没等他画完,另一个人已把蛇画成了,把壶抢过去说:“蛇本来是没有脚的,你怎么能给它画脚呢!”为蛇画脚的人,最终失去了酒。
但是蛇本来是没有脚的吗?并不是!这不,最近3月21日美国德克萨斯大学生物系领衔多所大学共同公布了草原响尾蛇(Crotalus viridis)的基因组,并从比较基因组学阐述了蛇类生物与蜥蜴来源于同一先祖,蛇原来以前也是带脚的。此外,还重点研究了蛇类性染色体的进化演变过程,以及微染色体结合蛇毒基因家族的进化事件,确定了染色质结构变化指导蛇毒基因家族的精确表达,并在转录调控层面加以补充论证蛇毒产生和调控机制。下面我们就来一起看看文章的内容细节吧:
实验设计
基因组样本:雄性草原响尾蛇肝脏。
转录组样本:草原响尾蛇16种不同组织,提取RNA,构建24个转录组文库。
Hi-C样本:分离毒液腺中毒液,提取DNA。
测序:Illumina,PacBio。
基因组组装、注释
最终组装响尾蛇基因组大小为1.34Gb,组装出18条染色体,contig N50为14.96Kb,Scaffold N50为179.898Mb。对组装基因组结果进行注释,预测到17,352个编码蛋白基因,重复序列39.49%。
表1草原响尾蛇基因组组装版本的基本信息
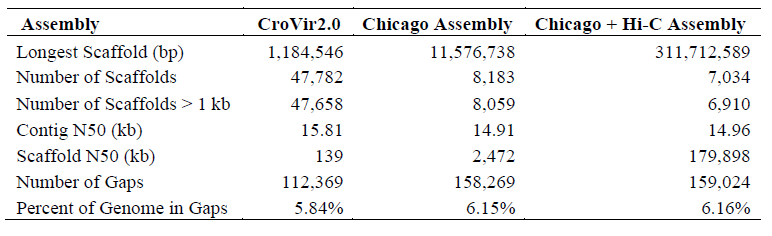
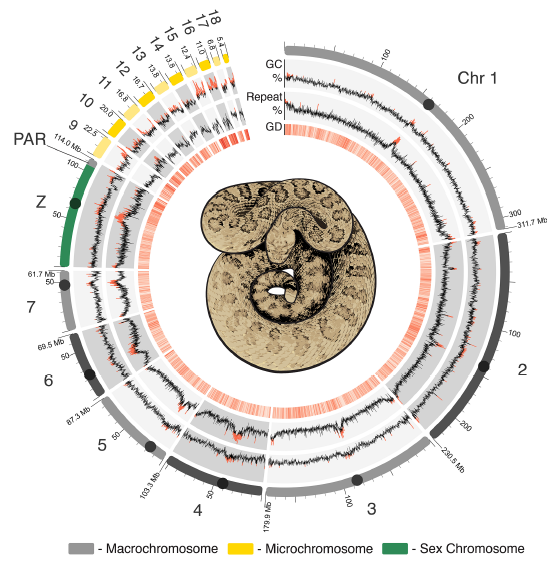
图1草原响尾蛇基因组图谱
染色体间共线性分析
通过共线性分析得到,大的同源区在染色体和微染色体之间存在重大转移,同时微染色体的GC含量高,具有的基因密度大(见图1)。在脊椎动物的大染色体上,染色质结构具有广泛的相似性,但蛇的微染色体具有独特的特征,响尾蛇大染色体上染色体内和染色体间染色质互作模式与哺乳动物中观察到一致,当染色体间互作频率按染色体长度归一化时,它们在物种间呈现一致的负线性关系。响尾蛇的微染色体明显偏离了这种大染色体模式,并与其他染色体(包括其他微染色体)有不成比例的高频率互作(图2A,B)。
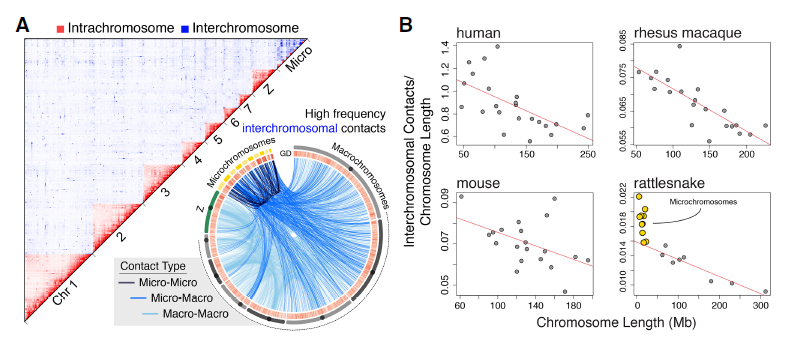
图2染色体间共线性分析图
基因组比较分析
对12种鳞类动物进行比较基因组学分析得到:响尾蛇与蜥蜴染色体高度同源(除了蜥蜴3号染色体融合/分离为响尾蛇4、5号染色体外),推断出百万年前两个物种来自共同祖先,很久以前蛇也是有腿的,但蛇类已经进化出更多的变异,其GC含量变化由AT偏移过程驱动,而不是靠丰富的GC累积。

图3 响尾蛇、鸡和蜥蜴基因组比较
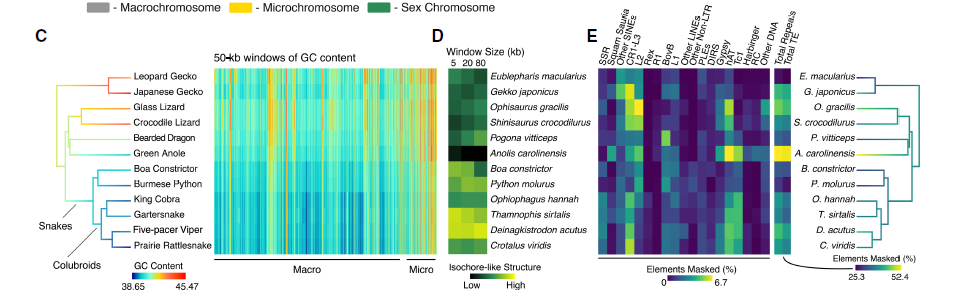
图4 12种鳞类动物基因组GC含量、重复序列比对
性染色体进化
确定一个114Mb的scaffold作为响尾蛇性染色体Z,Z染色体的重组伪常染色体区(PAR)确定为远端7.2 Mb区域(图5A);量化了预测的雌激素反应因子(EREs)的数量和Z染色体上100Kb窗口中F/M基因表达率的平均值(图5B),并用Pearson相关系数检验这些变量之间的关系,揭示Z染色体的进化与EREs的区域积累有关,这可能是区域剂量补偿的重要机制。
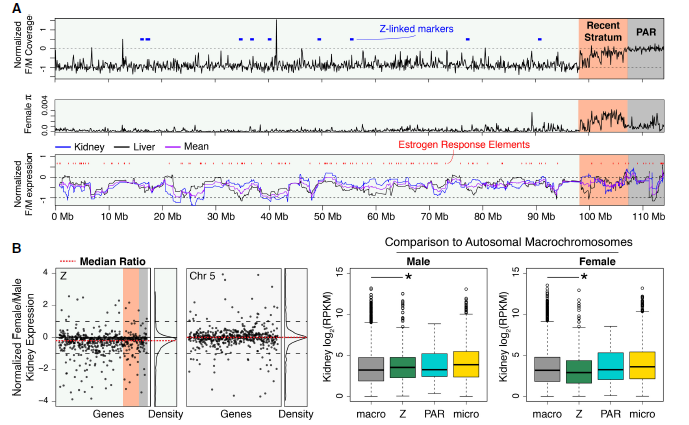
图5 响尾蛇Z染色体进化分析图
毒液基因家族分析
确定了蛇毒基因的基因组位置信息(图6),并表明这些基因在微染色体上富集(即37%的毒液基因存在于微染色体上,微染色体占基因组的10%)。此外,微染色体连接的蛇毒基因家族包括响尾蛇毒液中最丰富和特征最明显的三种成分(蛇毒金属蛋白酶,SVMPs;蛇毒丝氨酸蛋白酶,SVSPs;IIA型磷脂酶A2,PLA2s),每个家族位于不同的微染色体上。草原响尾蛇毒液的另一个主要成分肌毒(crotamine),位于染色体1上。利用38个已知蛇毒基因家族的代表,鉴定并注释了响尾蛇基因组中的蛇毒同源物。
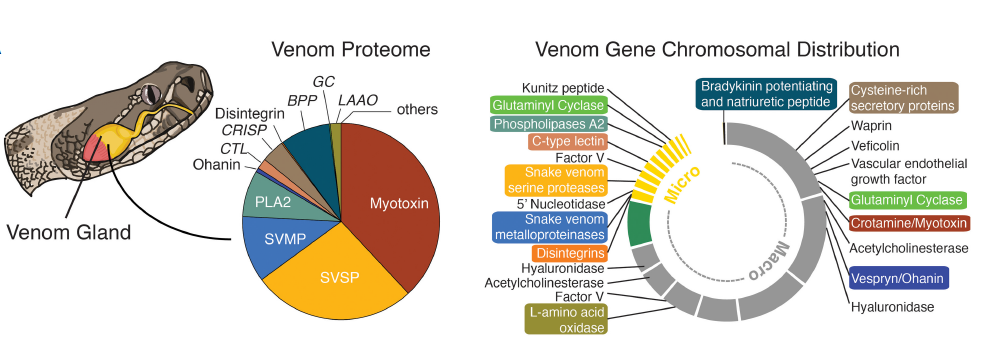
图6 蛇毒蛋白质组的饼状图及毒液基因家族的染色体定位
毒液调节机制
通过比较毒液腺体和机体组织之间的基因表达,发现12个转录因子(TFs)在毒液腺体中表达显著增高(图7B),但没有发现预测的结合位点的证据,表明它们在直接调节毒液基因中发挥作用。这里又对提取后的毒腺进行了Hi-C测序,使能够捕获与产生毒液有关的染色质互作关系,含有毒簇的基因组区域在离散的高频染色质接触区域内表现出一种特定的结构(TADs),这些蛇毒TADs的两侧是预测的CTCF结合位点,CTCF协调DNA循环并隔离转录活性(图7C,D),表明毒液簇区域周围TAD边界具有较强的绝缘调节作用。综上所述,论证了毒液基因调控是由紧密调控的染色质结构和对毒液耗竭反应的高表达TFs之间的协同作用驱动的。
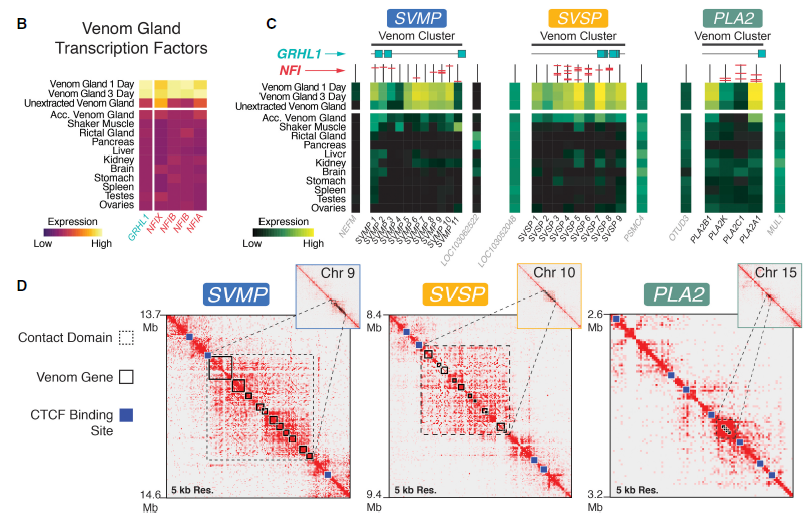
图7 转录因子及毒液基因在毒液腺体中的表达图、微染色体三维互作图
小结
作为第一个物种的微染色体使用Hi-C技术检测研究,发现了微染色体的独特结构和功能,并附带提出了一个问题:蛇的微染色体染色质结构的独特性是否是所有脊椎动物微染色体的共同特征?未来利用基因组数据或Hi-C手段来比较微染色体结构和核接触模式的分析将是解决脊椎动物谱系中微染色体结构、组织和功能之间联系的关键。
菲沙集成先进的三代测序技术平台和三维技术平台,全方位从基因组组装、分型,基因功能和进化研究为您助力基因组学研究,期望与各领域的专家合作,制定最优的解决方案,提供快速、准确、专业的服务,共同迎接生命科学研究中的挑战。
配图来源网络/侵删
参考文献:
Schield DR1, Card DC1, et al. The origins and evolution of chromosomes, dosage compensation, and mechanisms underlyingvenom regulation in snakes. Genome Res. 2019 Mar 21.
 微信公众号
微信公众号
