
急性病毒感染,例如流感,会引发病毒与免疫系统之间的竞争。当病毒传播时,一些细胞会产生干扰素(IFN),通过自分泌和旁分泌信号指导感染细胞及邻界细胞中抗病毒干扰素刺激基因(ISGs)的表达,从而激活体内广泛的免疫反应。如果先天免疫激活足够迅速, 则会降低病毒复制和疾病发生。由于流感病毒有很高的突变率,病毒基因的表达在感染细胞中差异很大,感染结果极不均匀,只有一部分感染细胞的先天免疫被激活。
相关研究表明流感病毒感染过程中只有一部分细胞的先天免疫被激活的两个重要因素在于纯粹的随机性和细胞状态中预先存在的变异。第三个关键因素是病毒的遗传多样性。而现有的流式细胞和荧光检测技术只能测定蛋白水平,单细胞转录组技术只能测定短片段转录本的丰度。这些技术均不能可靠地揭示感染细胞的病毒粒子是否具有某种特殊突变而不足以确定病毒遗传多样性如何在感染期间促进细胞间异质性从而激活先天免疫。
近期,美国西雅图华盛顿大学基因组科学系Russell等研究人员采用10X Genomics Chromium单细胞技术联合ISO-seq检测了感染细胞中所有流感病毒基因的完整转录本序列,发现感染细胞的病毒粒子在基因表达上有突变或缺陷。该研究同时确定了几种增加诱导IFN表达的病毒缺陷类型,且表明病毒多样性对于充分解释流感感染期间细胞间异质性是不充分的。相关结果以Single-cell virus sequencing of influenza infections that trigger innate immunity为题发表在Journal of Virology上。
流感病毒感染过程中,IFN在感染细胞中很少表达,研究者开发了一套独特的富集罕见IFN+细胞的流程,利用10x Genomics Chromium最终获取约1500个人肺部上皮细胞(IFN+和IFN-)分别进行单细胞RNA-seq及ISO-seq检测,umi标记的CCSs与illumina 3’端测序reads结合分析,可以确定单个细胞转录组及所有病毒基因的完整序列。
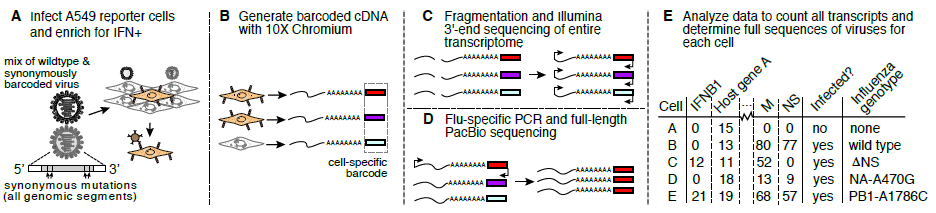
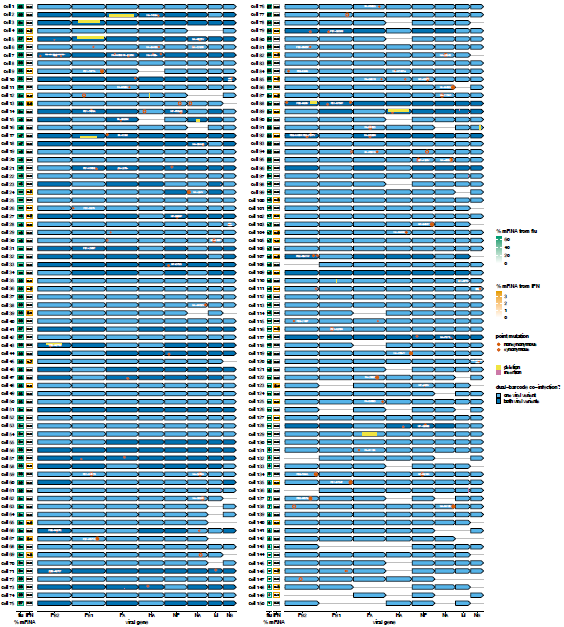
290个感染细胞中病毒mRNA分布非常不均匀:许多受感染的细胞只有来自病毒的百分之几的mRNA,但是病毒mRNA包含了细胞转录组的一半以上。其中162个细胞表达所有8个病毒基因。尽管病毒基因的绝对表达有很大的差异,但它们的相对表达是相当一致的。
病毒基因表达最高的感染细胞(其65%的mRNA来自病毒)中病毒粒子表达所有8个未突变的病毒基因,无法诱导IFN产生。其他12个细胞(至少有50%的mRNA来自病毒)被具有突变或无法表达病毒基因的病毒粒子感染,5个细胞产生IFN。所有病毒粒子感染的细胞都不能表达病毒聚合酶复合物的组分(PB2、PB1、PA或NP),因此病毒mRNA的表达量较低,因为它们仅限于利用进入的蛋白质进行初级转录。表达IFN最多的两个细胞缺乏编码NS基因。其他IFN+细胞也有不同的缺陷,如细胞内大量内部缺失或氨基酸突变。
为了系统的评估和感染结果相关的病毒特征,研究者选择150个感染细胞分为两组,一组表达所有8个未突变的病毒基因(不考虑同义突变),另一组不表达。病毒缺陷是造成病毒转录异质性的主要原因。一些病毒缺陷有助于诱导IFN的表达。不完全或完全突变的病毒粒子感染的细胞比表达所有未突病变病毒基因的病毒粒子感染的细胞表达IFN的频率更高,尽管这种差异在统计学上并不显著。而对于某些类型的病毒缺陷,IFN+细胞显著富集PB1中的NS缺失和氨基酸突变。总的来说,IFN+细胞中病毒基因表达增加,表明自分泌IFN信号通常发生得太晚,无法抑制病毒转录。单个IFN+细胞中发现的病毒缺陷可导致IFN表达增加。
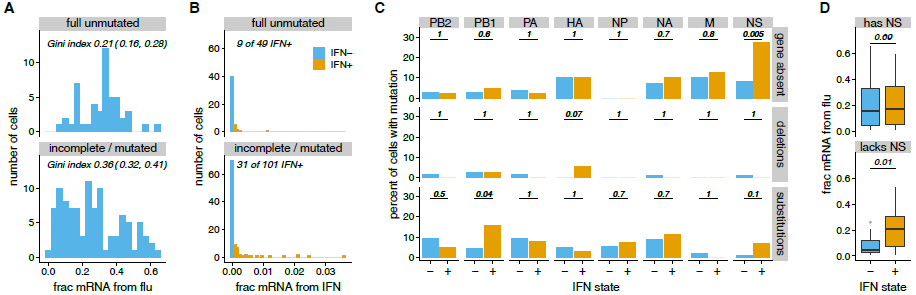
在单细胞中识别的不同范围的免疫刺激病毒缺陷通过不同的过程起作用,病毒的变异不仅影响诱导IFN表达的速度,而且影响诱导IFN表达的因素。
人类流感感染是由少数病毒粒子建立的,这些病毒粒子随后经历指数级增长,通过旁分泌信号放大早期IFN反应。早期的先天免疫诱导异质性可能会影响整个感染过程。本研究最大价值不仅仅是对诱导IFN表达的病毒缺陷的筛查,更是对单个感染细胞中病毒变异的详细调查。任何病毒缺陷均没有诱导IFN表达的特定途径。病毒遗传缺陷并不能完全解释感染细胞之间的异质性,随机的或预先存在的细胞状态也在先天免疫诱导中发挥重要作用。
原文链接:https://jvi.asm.org/content/early/2019/05/02/JVI.00500-19
 微信公众号
微信公众号
