
RNA聚合酶(RNAP)是以转录DNA的能力而闻名的分子马达,RNAPII和染色质的结合与空间相互作用的形成差异之间存在某种联系。除了潜在的直接影响,RNAP和转录行为还可能通过与黏连蛋白-CTCF复合物的相互作用来重塑基因组折叠。此外,RNAP对于结构域形成是必不可少的,并且经常被凝聚素复合物抵消。因此需要剖析和协调RNAPII对染色质结构的贡献。
概 述
有丝分裂诱导显著的染色体压缩,但在重新进入G1期后染色体重新建立其间期组织。由于RNAP的药理学抑制效率低下,德国哥廷根大学医学中心和英国爱丁堡大学等合作研究团队开发了允许生长素介导的人类细胞系,可以快速和可逆地消耗RNA聚合酶II(RNAPII) ,用以测试RNAPII在这种状态转变中的作用。原位Hi-C表明RNAPII是有丝分裂后compartment和loop建立所必需的。RNAP通常会抵消loo挤压。如果没有它会出现更长、更突出的loop。而来自染色质结合、超分辨率成像和计算模型的证据暗示这些效应是由于再进入G1时RNAPII介导黏连蛋白加载。该研究利用多种组学技术,将RNAPII在基因表达中的作用与染色质结构中的作用协调展示。
(原文链接:https://www.science.org/doi/10.1126/sciadv.abg8205)

研究策略
研究材料:人DLD-1结直肠癌系,大肠癌细胞系HCT116
研究方法:
测序技术:Hi-C,ChIP-seq,ATAC-seq,CUT&Tag,Factory RNA-seq(新生RNA水平)
定量、成像技术:蛋白质印迹,双色超分辨率dSTORM荧光免疫技术,FACS分选,3D-DNA FISH
计算建模:HiP-HoP模型和ENCODE公共数据
研究思路
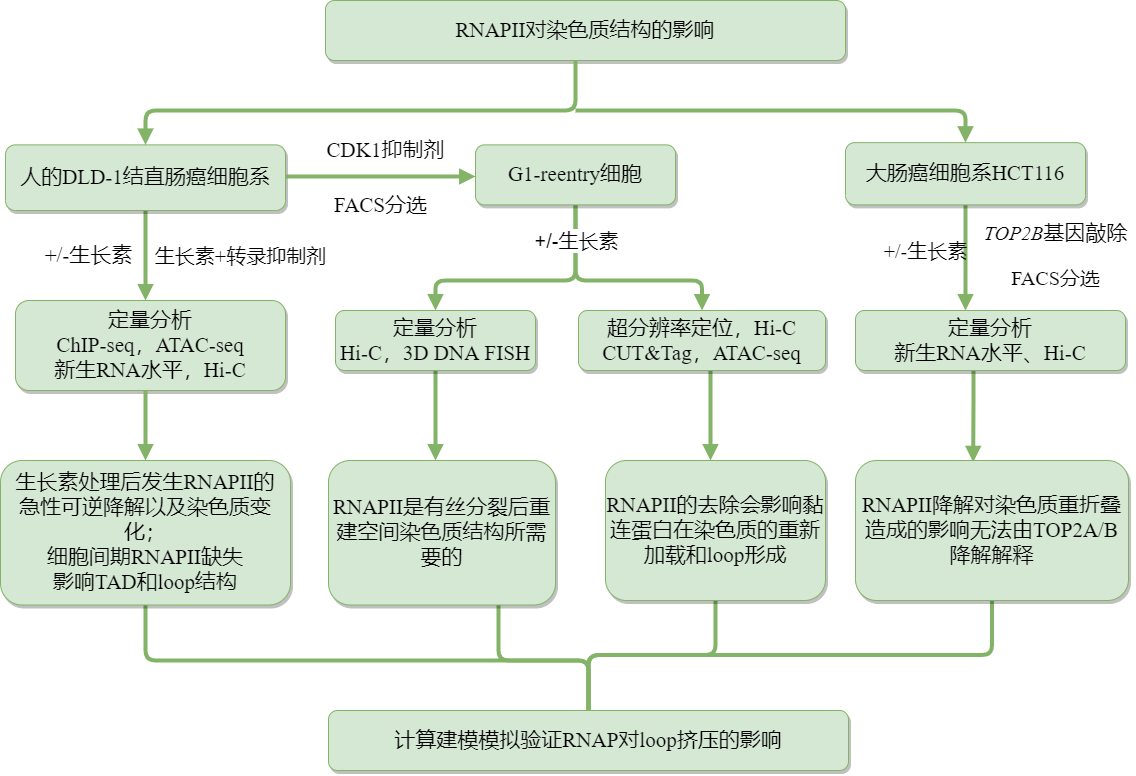
研究结果
1、RNAPII的严重缺失影响loop水平的染色质结构
RNAPII对细胞活力至关重要,其耗尽可能仅是瞬态的。研究者利用了人的DLD-1结直肠癌细胞系,它最大的RNAPII亚基RPB1是mAID结构域的N-端标记,可以添加生长素(和多西环素dox)以激活植物泛素连接酶TIR1来识别该mAID结构域,联合蛋白质印迹评估、ChIP-seq(RPB1中mClover蛋白,RNAPII,H3K27ac,H3K27me3)、ATAC-seq和Factory RNA-seq确认dox/生长素处理后发生RNAPII的急性、可逆降解,并且还伴随着染色质开放性剧烈减少,活性染色质显著减少和兼性异染色质水平升高,>90%新生RNA下调且主要参与染色质组装和基因表达调控。
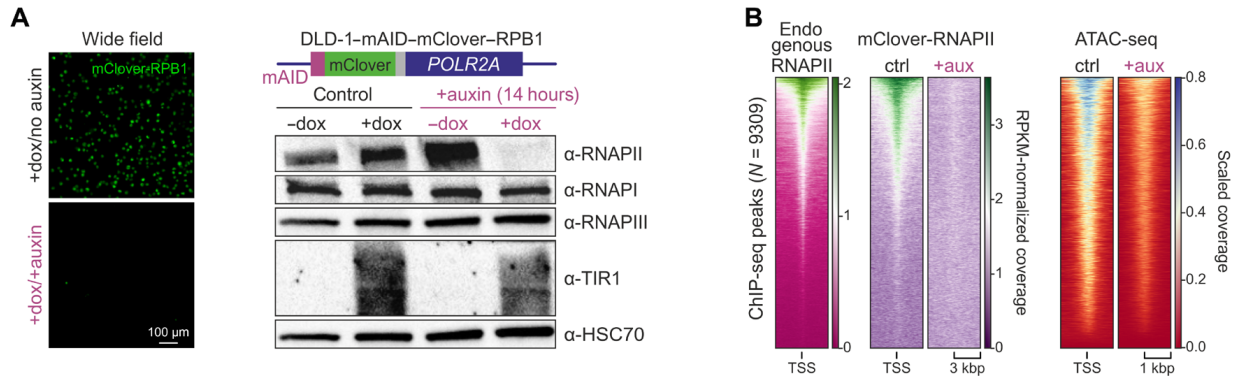
图1 生长素处理后发生RNAPII的急性可逆降解
随后,研究者关注RNAPII耗竭时细胞间期染色质的空间结构变化,利用Hi-C技术分析有无生长素处理、以及在生长素基础上补充转录抑制剂雷公藤内酯处理的G1-sorted DLD-1–RPB1–mAID细胞,结合生长素/雷公藤内酯处理后增大的loop内累积新生RNA水平,结果显示活性RNAPII可以抵消loop挤出,其去除会导致loop扩大。并且mAID-RPB1细胞在用生长素处理后染色质空间结构无变化,细胞间期急性RNAPII缺失时发生有微妙但可辨别的TAD和loop结构水平变化。
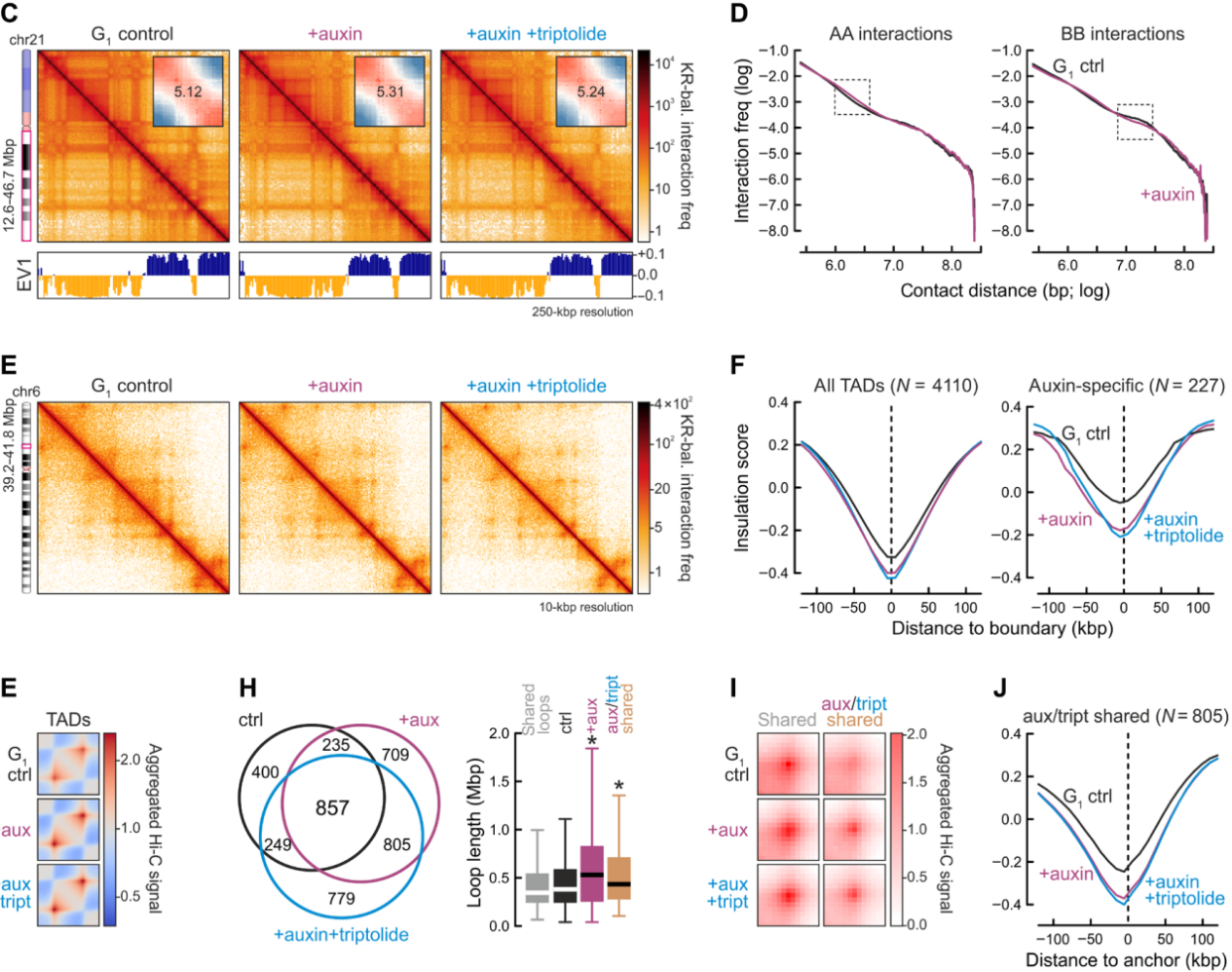
图2 RNAPII耗竭时细胞间期染色质的空间结构变化
2、RNAPII是有丝分裂后重建空间染色质结构所需要的
RNAPII没有显著地影响异步细胞群中的间期染色质结构,研究者假设它可能与有丝分裂后重建染色质折叠有关。研究团队为此使用CDK1抑制剂(阻断约90% G2细胞)在G2-M checkpoint同步mAID-RPB1细胞,然后通过有丝分裂进入G1并利用FACS分选得到G1-reentry细胞。多种定量分析发现添加生长素确实发生RNAPII耗竭,H3K27ac水平降低,H3K27me3水平增加,同时SWI/SNF染色质重塑亚基改变,CTCF不变。接下来分析添加生长素RNAPII缺失后发生的染色质空间结构变化:
对用或未用生长素处理的G1-reentry细胞进行Hi-C,结合3D-DNA FISH证实RNAPII降解引起染色体间互作增强而染色体内互作减弱,compartment边界模糊,A和B comptment之间>1Mb的互作更强。
10kb分辨率Hi-C分析,在生长素处理的细胞观察到强烈且广泛的domain结构、局部insulation和loop形成的缺失,边界塌陷以及TAD合并。这与RNAPII和TAD边界组蛋白标记的富集变化一致。
RNAPII缺失引起的loop水平变化,大约有1900个丢失,同时出现>1150个新的和明显更长的loop。
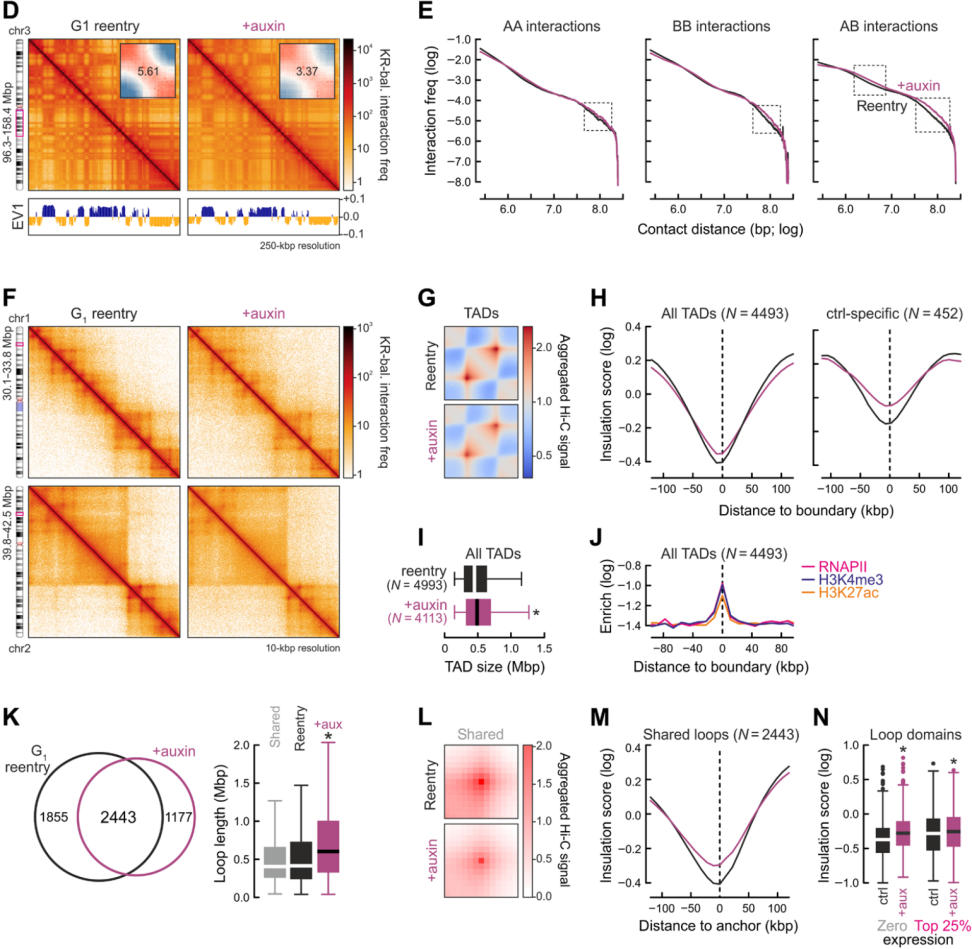
图3 添加生长素RNAPII缺失后发生的染色质空间结构变化
3、拓扑异构酶II消耗不影响G1-reentry期细胞的染色质折叠
考虑到拓扑异构酶(TOP2A/B)对RNAPII动态的局限影响,研究者想确定G1-reentry细胞中TOP2缺失是否可以解释RNAPII缺失所产生的影响,因而应用携带/未完全敲除TOP2B基因并纯合表达mAID-tagged TOP2A的大肠癌细胞系HCT116。先验证了生长素对TOP2A/B的降解作用,联合FACS得到G1-reentry细胞,并分析新生RNA水平以及所有层级染色质结构的变化。多种数据分析表明RNAPII降解对染色质重折叠造成的影响无法由TOP2A/B降解概括,而是以聚合酶为中心。
4、RNAPII的去除会影响黏连蛋白在染色质的重新加载和loop形成
鉴于G1-reentry细胞在RNAPII缺失时发生的loop变化以及影响loop形成的因素(CTCF锚定处的cohesin复合物和挤压DNA),研究者利用多个分馏蛋白质印迹以及免疫荧光定量技术,检查显示CTCF、SMC1A或Rad21在生长素处理后reentry细胞中发生细小波动,两个cohesin loader(NIPBL和MAU2)和黏连蛋白释放因子(WAPL)的染色质结合水平则显著降低。其后在有无生长素处理的G1-reentry细胞中,利用超分辨率定位技术查看NIPBL和CTCF位置并结合染色质上NIPBL/MAU2/WAPL的水平变化,猜想黏连蛋白在没有RNAPII的情况下加载异常(最有可能是从染色质释放),并且CTCF结合位点的黏连蛋白减少。
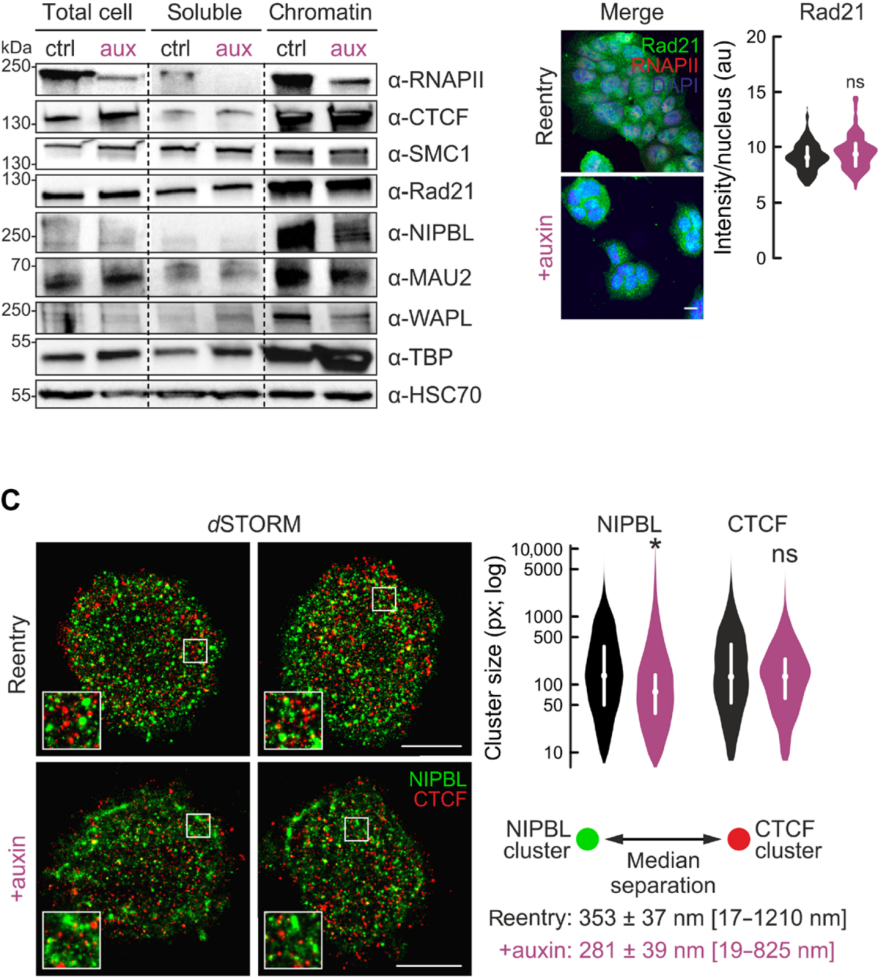
图4 RNAPII的去除会影响黏连蛋白在染色质的重新加载
因此,研究者在对照和生长素处理的reentry细胞中进行CUT&Tag(SMC1A和Rad21),发现CTCF位点的黏连蛋白信号在全基因组水平显著降低,进一步量化CTCF结合区域、活性或非活性TSS和非RNAPII相关基因CUT&Tag信号以及Hi-C分析显示,这种CTCF结合位点上黏连蛋白占有率的普遍减少损害了全基因组的loop形成。值得注意的是,此时ATAC-seq显示CTCF近端可及性没有降低。并且在RNAP耗尽的细胞中TSS的ATAC-seq信号和染色质上的TBP(TATA box–binding蛋白)水平增加,而RNAPII/SMC1A共占的TSS处CUT&Tag信号显著降低,同时再次结合定量分析发现RNAP将黏连蛋白loader和释放因子招募到这些位点,而在G1-reentry细胞中建立TSS结构可能依赖于形成聚合酶前的“先锋”因子(如TBP之类)。
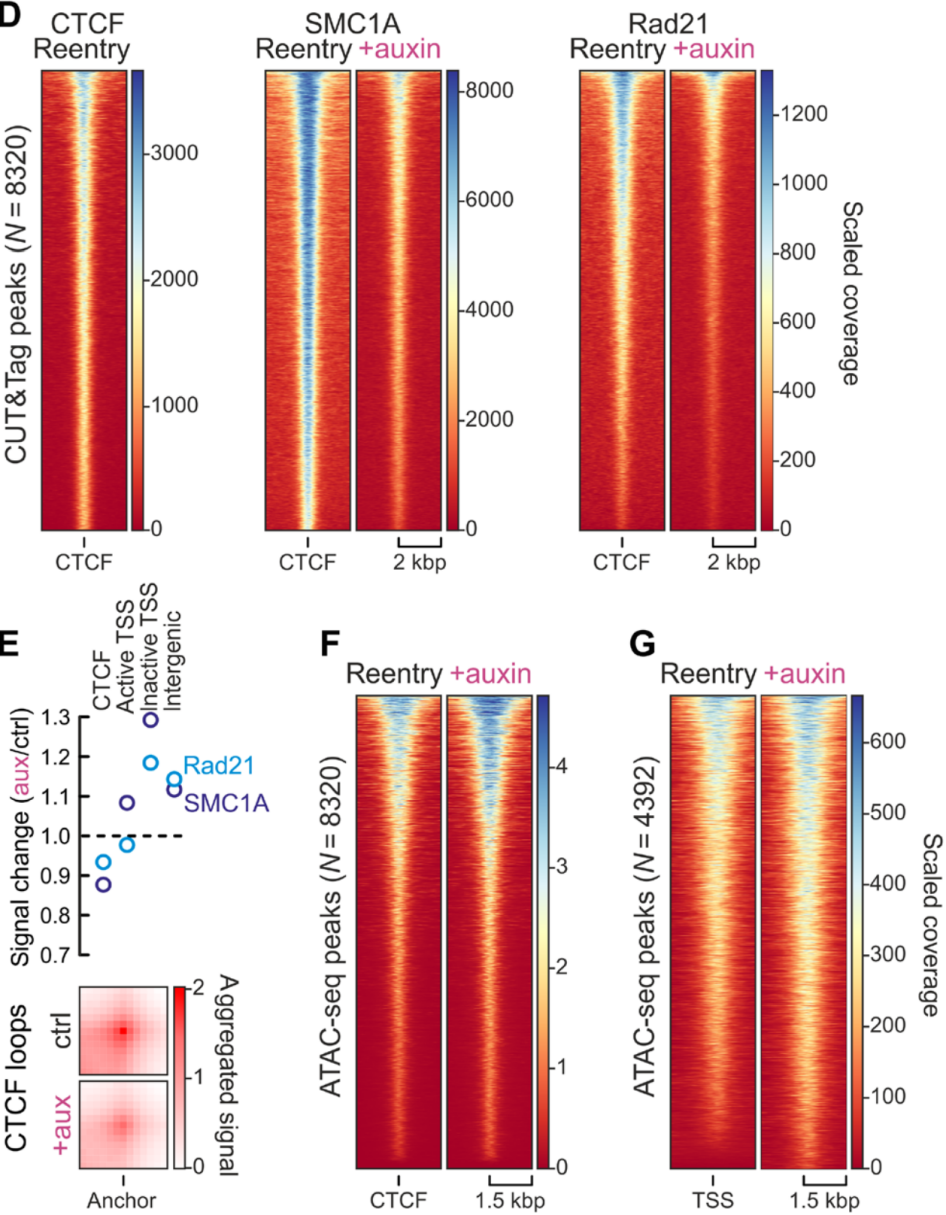
图5 RNAPII的去除会影响黏连蛋白在染色质的重新加载和loop形成
5、RNAP对loop挤压的建模剖析
最后,该研究利用计算模型构建实验难以挑战的场景来剖析RNAPII和黏连蛋白重新加载到染色质上之间的联系。主要是使用HiP-HoP模型调控多种情景下的三维染色质折叠,基于公共数据阐释染色质的异常性质并整合TF结合和loop挤压。通过多种参数调整,建模表明实验中的主要染色质折叠差异可以通过RNAPII结合位点无法加载黏连蛋白来解释,并且推断出实验中观察到的效果可以通过RNAP占据位点的黏附蛋白与转录活性和loop挤压之间的相互作用之间的简单关系来说明。
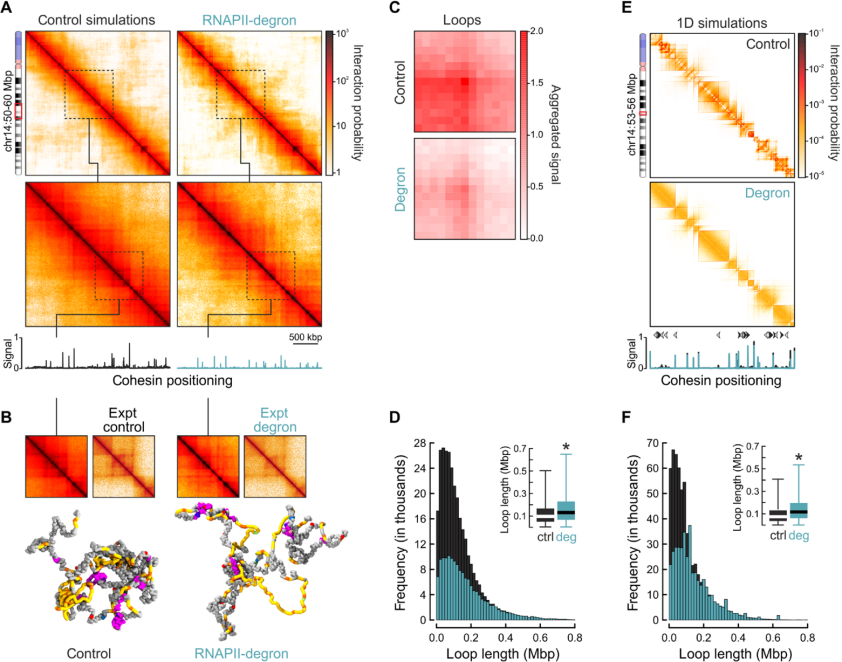
图6 建模剖析RNAP对loop挤压的贡献
永利集团3044提供多种表观技术服务,类型包括Hi-C、Hi-R(RNA-RNA互作)、Capture Hi-C 、ATAC-seq、CUT&Tag、3C、Tn5-FISH、WGBS等。永利集团3044已成功完成了包括人类、动植物、微生物在内的数百个物种数千个项目的实验及数据分析服务,研究成果在《Nature》、《Cell》、《Cell Research》等国际顶级期刊发表几十余篇。永利集团3044期望与各领域的专家合作,提供专业细致的服务,共同攀登生命科学研究高峰。
参考文献:
Zhang S, Uebelmesser N, Josipovic N, et al. RNA polymerase II is required for spatial chromatin reorganization following exit from mitosis[J]. Available at SSRN 3726273, 2020.
 微信公众号
微信公众号
