
#
产品介绍
单细胞测序已经给医学科研领域带来了革命性的进展,当下应用最火热的是10× Genomics公司的解决方案,但该技术无法满足某些特殊或者少量细胞样本。Smart-seq2技术可应用于细胞分子机制中细胞异质性研究以及解决了因样本量少而无法进行高通量测序的情况。
Smart-seq2技术于2013年公布,在单细胞水平对带poly(A)尾巴的RNA分子(主要为mRNA)进行转录组全长扩增及高通量测序的一种高端技术,具体方法采用改进的Smart-seq2技术,能够满足高灵敏度、低偏好性的cDNA扩增,对转录本的整体覆盖情况进行了完善,实现了高水平的序列模板转换。在分析不同细胞间差异表达之外,还能深入检测到细胞内融合基因,可变剪切,基因位点突变等信息。
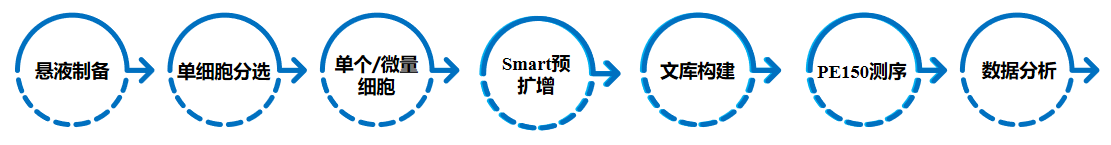
Smart-seq2单细胞转录组技术流程图
#
Smart-seq2测序流程
(1)分离出单细胞,并用裂解液裂解细胞。
(2)在裂解液中加入MMLV逆转录酶、游离的dNTPs、oligo(dT)VN Primer、甜菜碱、MgCl2等,通过oligo(dT)VN Primer启动mRNAs反转录,获得cDNA第一条链。
(3)RT反应通常在42°C进行90分钟,但是某些RNA形成二级结构(例如发夹或环),由于空间位阻,可能导致酶终止链延长。通过添加海藻糖和甜菜碱,可以在某种程度上克服这种不良影响。
(4)当反转录到达RNA5’末端后,MMLV逆转录酶的末端转换活性会在cDNA末端加非模板编码的核苷酸,通常是dCTP。
(5)加入模板转换引物TSO,当反转录到达mRNA的5’末端,TSO3’的r(G)3和cDNA序列中富含dC的序列依靠互补作用促进模板转换。MMLV反转录酶会转录这个寡核苷酸序列,进行后续PCR扩增,获得双链cDNA。
(6)cDNA合成之后,加入常规PCR引物,进行常规PCR扩增,将扩增的cDNA打断,构建标准的Illumina测序文库。
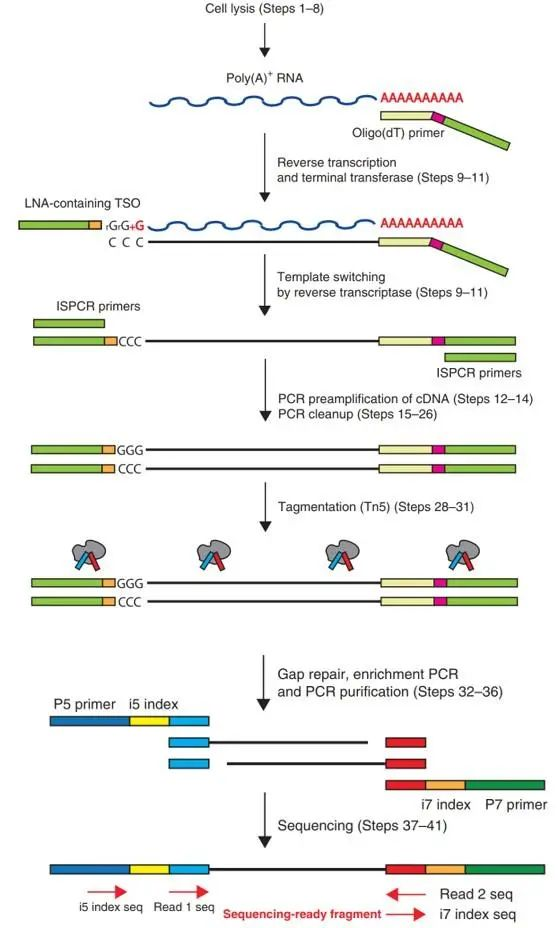
Smart-seq2建库技术流程图
#
技术优势
(1)模板起始量低:1-1000个细胞或10pg-10ng total RNA即可作为起始模板,进行高效扩增;
(2)转录本覆盖度高:通过双端引物扩增全长cDNA,获得全转录组信息,避免3端和5端偏好性,产物完整性好;
(3)检测灵敏度高:大幅度增加了低表达基因的检出量
(4)碱基分辨率高:可达单碱基分辨率,且可以定位到具体基因的具体转录本
(5)实验可控:质控点多,可从实验的开端判断细胞状况。
#
送样细则
(1)从组织分离单细胞,要求是新鲜的组织,没有经过冷冻、固定等处理。保证细胞活性和形态完整,不要损伤细胞。
(2)分离的单细胞放入公司提供的裂解液中,200 uL pcr管含有n个反应的单细胞裂解液,由于分装过程可能存在损耗,建议做(n-1)个样品。
(3)使用前冰上冻融,微型离心机/掌上离心机离心5-10 s,再向单细胞转录组裂解液加入单细胞溶液。
(4)含单细胞溶液的体积在0.5-1 uL之间。(加入5 uL裂解液后总体积在5.5-6 uL)
(5)实验操作尽量在冰上操作。
(6)单细胞加入裂解液后低速离心,确保细胞不会挂在管壁。液氮速冻后干冰寄送。
#
应用研究
(1)免疫学研究:免疫学研究中针对少量分选的细胞,再通过Smart-seq2技术扩增出每个单细胞全长转录本,从而获得基因表达及VDJ的数据,针对分析不同抗原的免疫细胞的特异性表达情况[1]。
(2)肿瘤及微环境研究:癌细胞由于基因突变和表达谱不同而产生的癌细胞亚型,这些肿瘤内部不同的细胞亚型对于癌症患者的诊断和治疗带来极大的挑战,借助分选技术分选出不同亚型的肿瘤细胞进行Smart扩增,获得不同亚型肿瘤细胞的基因表达数据,借助已知的基因marker可以对这些亚型进行识别,为癌症的临床治疗提供精准的基因及转录本层面的数据[2]。
(3)绘制组织精细化表达图谱:Smart-seq2可与10×Genomics联合,弥补其对于单个细胞基因表达测定信息不全的缺陷,实现了对特定细胞的更高精准度的转录本覆盖,进而可以绘制精细的单细胞表达图谱[3]。
(4)早期胚胎发育:早期胚胎发育形成的细胞数量及其有限,Smart-seq2技术可以借助有限的细胞分析胚胎发育过程中的不同阶段的基因表达的差异,早在2009年,汤富酬首次分析了体外囊胚期内细胞团向多能胚胎干细胞转变过程中转录组重编程的过程[4]。
参考文献:
[1] Björklund ÅK, Forkel M, Picelli S, et al. The heterogeneity of human CD127(+) innate lymphoid cellsrevealed by single-cell RNA sequencing. Nat Immunol. 2016;17(4):451–460.
[2] Zhang Q, He Y, Luo N, et al. Landscape and Dynamics of Single Immune Cells in Hepatocellular Carcinoma. Cell. 2019;179(4):829–845.
[3] Haber AL, Biton M, Rogel N, et al. A single-cellsurvey of the smallintestinal epithelium. Nature, 2017;551:333–339.
[4] Tang F, Barbacioru C, Wang Y, et al. mRNA-Seq whole-transcriptome analysis of a single cell. Nat Methods. 2009;6(5):377–382.
 微信公众号
微信公众号
