
“异香飘溢岚风口,根白苍黄布满天”,作为中华民族的传统瑰宝,中草药在国民健康和经济振兴道路上起着重要作用。在我国中医药源远流长的历史长河中,湖北中药材扮演着举足轻重的角色。神农故里,药圣故乡,被称为“华中药库”的湖北中药材,名不虚传。而近期公布的“十大楚药”(蕲艾、半夏、天麻、黄连、茯苓、福白菊、苍术、龟鳖甲、银杏、紫油厚朴、黄精),更是湖北中药资源中的“名之贵品”。
自2010年公布首个中草药“丹参”基因组以来,12年间,基因组测序在解析中草药的药用成分和适应性机制方面发挥了重要作用。基于此,小编以“十大楚药”为例,系统梳理12年来中草药基因组研究的经典思路,以飨读者。
1
经典思路一:药用成分的生物合成机制解析
01
两篇黄连基因组,揭示小檗碱型生物碱生物合成机制

黄连是一种珍贵的中药材,其在心血管、糖尿病等的防治中具有重要作用。黄连的药用成分主要是小檗碱、黄连碱、药根碱、等原小檗碱类生物碱。
2021年6月,Horticulture Research在线发表了黄连染色体水平的参考基因组,其基因组大小为958.20Mb,contig N50=1.58Mb;研究发现,LTR反转录转座子扩增是引起黄连基因组变大的主要原因;比较基因组学分析表明,与生物碱合成相关的基因在黄连中显著扩张天冬氨酸转氨酶基因(ASP5)在小檗碱代谢途径中被显著正选择;在黄连的第三年和第四年中,生物碱含量最高。总之,本研究为黄连次生代谢产物的生物合成研究提供了新见解。
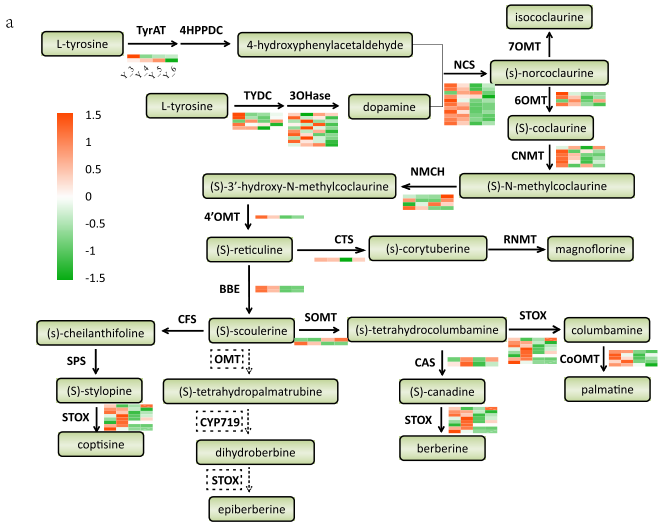
图1 黄连中BIA的生物合成途径
2021年6月,NC发表了味连的染色体水平基因组,基于该基因组,研究者全面分析了黄连生物碱合成相关基因的分布方式和进化途径。结果表明,CYP719家族的P450基因在黄连的生物碱多样化过程中起到了关键作用,其多数家族基因在黄连以串联重复的方式排布,包括小檗碱合成关键基因CAS。基于酵母表达的底物催化功能验证,发现CAS可能存在多样化的底物催化功能,可参与到黄连生物碱合成的多个途径或步骤。
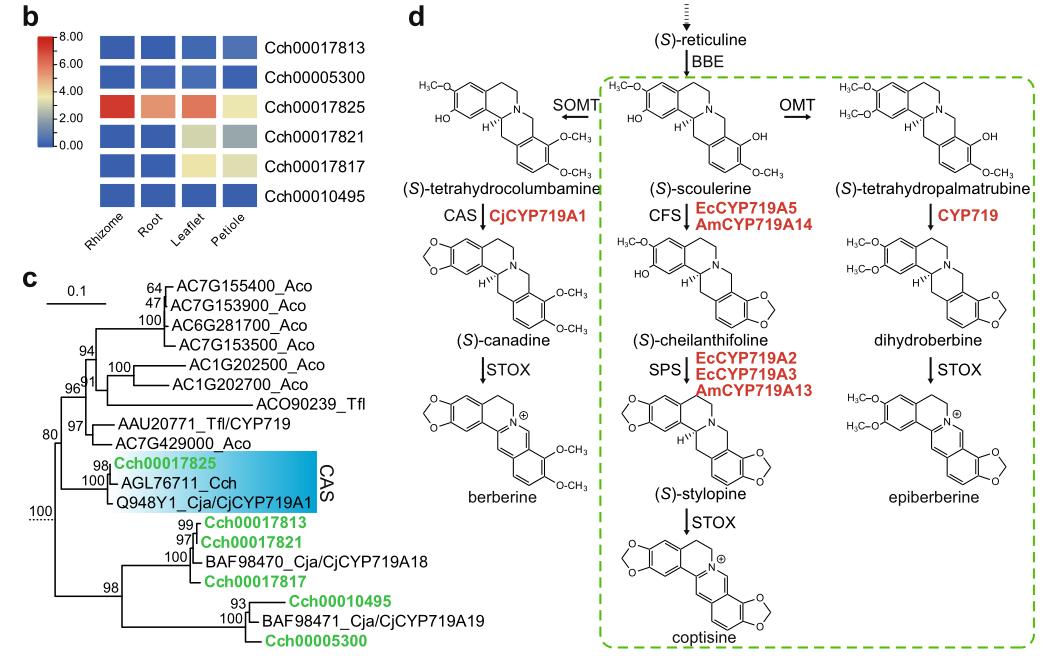
图2 黄连CYP719基因家族的进化
2
经典思路二:中草药环境适应性机制解析
01
天麻基因组揭示其菌异养的适应性机制

天麻(Gastrodia elata)是我国传统名贵中药材,对儿童惊风、头痛眩晕具有良好功效。同时,天麻也是典型的菌类异养植物,是研究寄生适应性的模式物种。
2018年,NC基于二代测序发表了天麻基因组的草图,结果发现天麻经历了广泛的基因缺失事件,甚至包括20.4%的高保守基因。但天麻的线粒体基因组却经历了显著的扩张至1339Kb,这些结果可能是天麻适应异养生活方式所导致的,这也揭示了异养植物的基因组具有较大的可塑性。
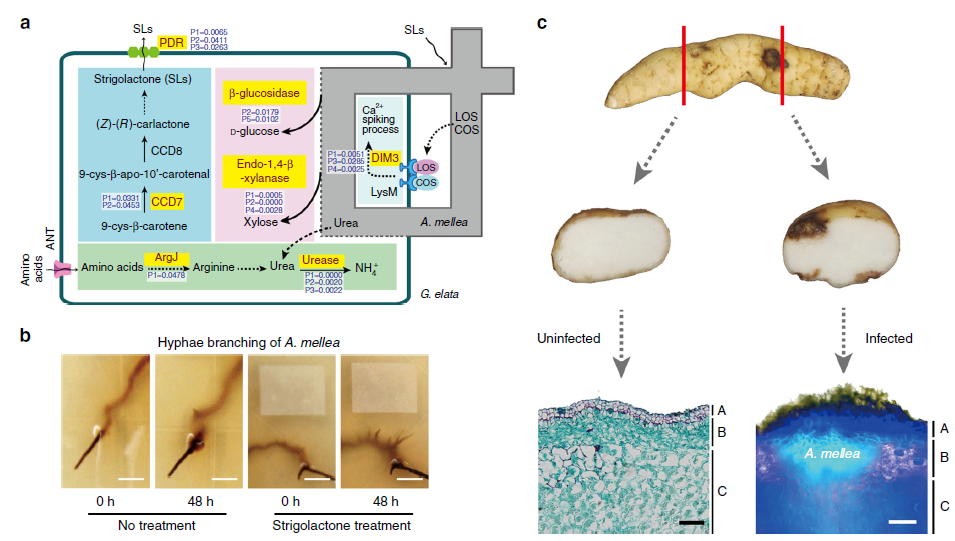
图3 天麻与蜜环菌共生机制解析
2021年10月,the plant journal发表了基于三代测序的天麻染色体水平基因组。通过将天麻与独脚金、菟丝子等植物进行比较分析,研究者发现天麻丢失了10%的保守基因家族,基因家族收缩程度与植物异养习性密切相关;在完全菌异养和全寄生植物中,存在着基因丢失的趋同进化,包括涉及光合作用、生物钟、开花时间调控等基因。这说明,异养生活方式的植物,其基因丢失与生理变化可能是为了适应其生存环境与生存习性。
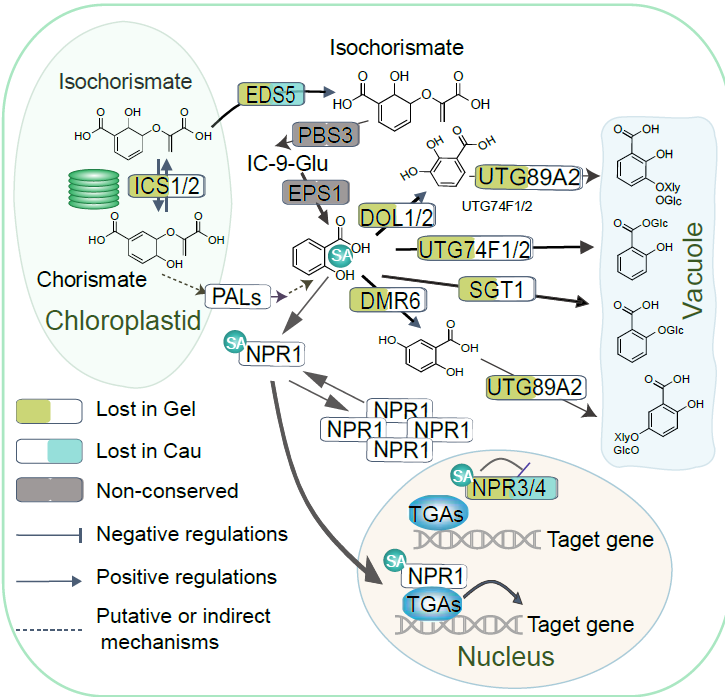
图4 天麻基因丢失情况
3
经典思路三:多物种比较揭示中草药的系统发育与进化地位
01
厚朴基因组为木兰类系统发育提供新见解

厚朴(Magnolia officinalis)是木兰科具有代表性的高大芳香树,是一种药用植物,广泛应用于从医药到化妆品的多种行业中。
2021年8月,iscience公布了厚朴的染色体水平基因组,其基因组大小为1.68Gb。研究者发现高比例的重复序列是木兰科植物的共同特征。木兰是真双/单子叶植物的姊妹分支,这为理解被子植物的系统发育位置提供了更多支持。一个古老的复制事件发生在药用樟科植物的基因组中,并与樟科植物共享。基于RNA序列分析,研究者确定了基因组中与木脂素生物合成相关的几个关键酶编码基因家族。总之,厚朴基因组为木兰类的进化研究提供了新见解。
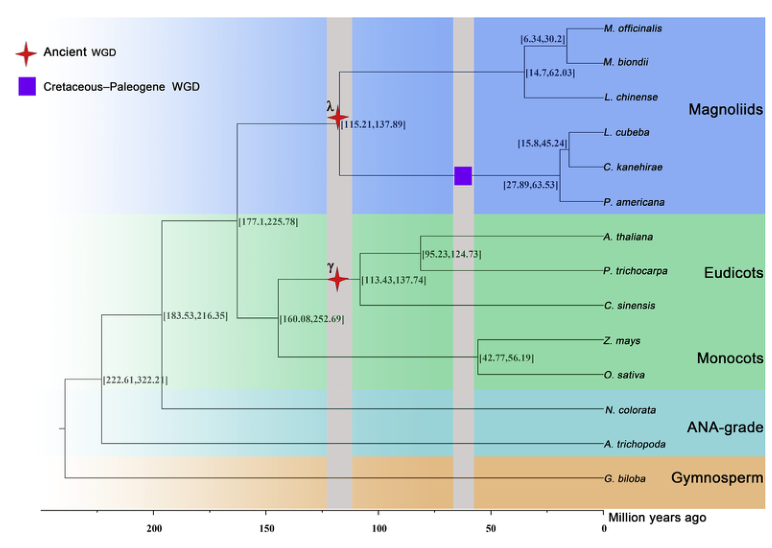
图5 厚朴的系统进化分析
02
蕲艾基因组为其核型演化研究提供了新见解

蕲艾(Artemisia argyi)是菊科多年生植物,是我国著名的地道药材,其不仅在中药方面有广泛用途,在日用、生活、添加剂方面也有广泛应用。
2022年6月,PBJ在线发表了蕲艾的染色体水平基因组,其基因组大小为8.03Gb,contig N50=6.25Mb,并发现其近期发生了3次WGD事件,这可能是导致蕲艾基因组超大的主要原因。艾染色体基数和倍性一直存在争议,通过深入分析,研究者发现艾染色体基数为17条,总数为34条,且蒿属祖先的8、9号两条染色体融合形成10号染色体。这说明,染色体融合是蒿属植物染色体进化过程中的关键机制。总之,本研究为蕲艾及蒿属亲缘关系研究提供了新见解。

图6 蕲艾存在染色体融合事件
4
经典思路四:多组学解析特殊表型形成的分子机制
01
银杏基因组揭示其“孑遗”性状的形成机制

银杏(Ginkgo biloba)隶属银杏科银杏属,是中生代孑遗的稀有树种,系中国特产,同时也是珍贵的用材树种,其花语象征着长久守护的爱、坚强不屈的精神和沉着稳定的魅力。
2016年发布了银杏基因组的草图,2021年6月Nature Plants基于三代测序了发布了高质量的银杏染色体水平基因组,研究者组装的银杏基因组大小为9.88Gb(contig N50=1.58Mb),注释得到27832个蛋白编码基因。在研究的植物种类中,银杏基因组内含子的长度是最大的,这进一步说明重复序列不仅促进了基因组的扩展,而且增加了蛋白质编码基因的大小和复杂性。
基于该基因组,同时结合转录组等多组学数据初步解析了银杏保留的精子鞭毛、未成形的花、扇形的叶等特殊性状的形成机制。结果表明,精子鞭毛的产生可能是由于控制和调节鞭毛生物合成的基因在银杏中得以保留;银杏中不存在花器官特征基因的同源物,表明花MADS-box基因在被子植物共同祖先中的扩张确实与花起源密切相关;银杏包含更少的器官极性基因,这些基因资源的缺乏和萎缩导致了扇形叶子的形成。
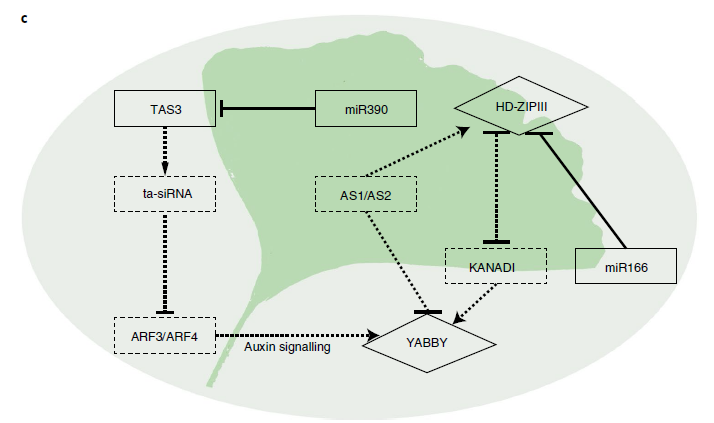
图7 银杏扇形叶形成机制的解析
5
经典思路五:群体基因组学对重要性状相关的基因进行定位
01
群体多组学分析揭示茯苓的遗传多样性与高产相关基因

茯苓(Wolfiporia cocos)隶属于多孔菌科,是世界著名的褐腐菌,具有重要的经济与药用价值,其干的菌核是中药中名贵的原料药。
2020年,Genomics Proteomics Bioinformations对茯苓进行了基因组与转录组学研究,揭示了茯苓菌核的形成机制。研究者鉴定到了2838个与菌核发育相关的差异表达基因,包括交配过程的基因、子实体组织分化和代谢途径;进一步,研究者也确定了几个参与药用特性相关的生物合成基因。
2022年,结合基因组、群体基因组、转录组分析,研究者揭示了39份茯苓的遗传多样性,结果表明茯苓可以分为3个类群,在主产区种植的茯苓可能有共同的起源;与茯苓产量相关的候选基因主要富集于氧化还原和碳水化合物代谢途径中,并且这些基因在最高产量的茯苓株系中得到高度表达。总之,本研究为茯苓种群结构和高产相关基因研究提供了新见解。
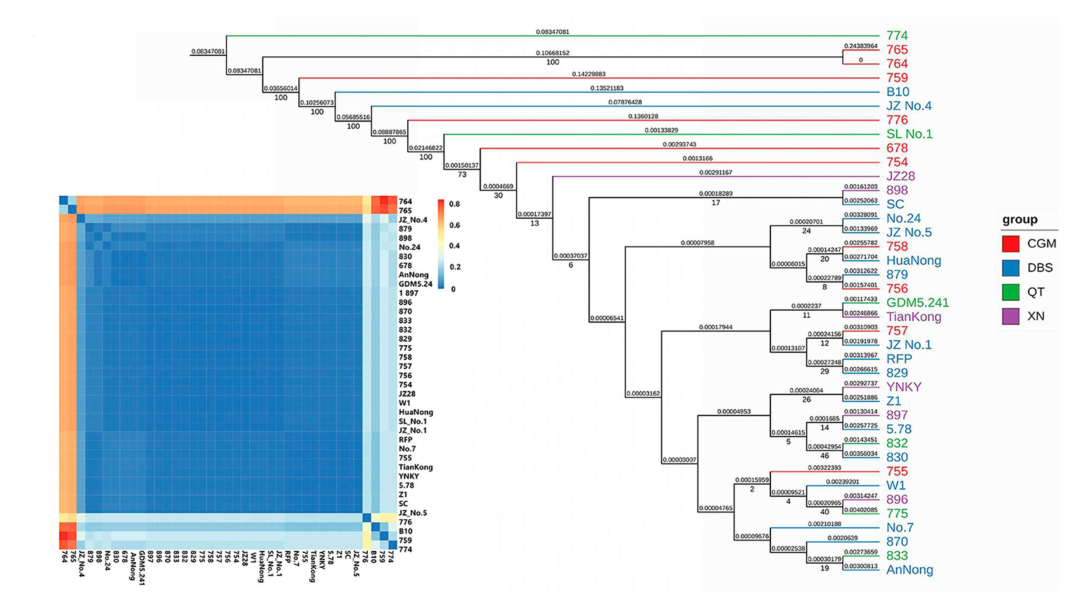
图8 茯苓的种群结构分析
总 结
以中草药为主的本草基因组学在过去12年里得到了极大发展,许许多多已公布的基因组为中草药的药理、生理、资源研究提供了重要理论基础。而展望未来,本草基因组学在选材上会越来越注重地道药材(例如十大楚药),在组学层面会越来越注重多组学的联合分析(基因组、转录组、代谢组、表观组、微生物组),在生物学故事的解析上会越来越聚焦于下游的应用。
永利集团3044在本草基因组学中拥有丰富的项目经验,累计参与发表中草药相关文章20多篇,累计影响因子突破150+,其中共同作者发表的黄花菜基因组更是被新闻联播所报道。菲沙近期协办的第五届武当国际医学论坛暨“十大楚药”之黄精产业发展研讨会为黄精的科研与产业发展起到了重要推动作用。在以十大楚药为例的地道中药材多组学的发展道路上,永利集团3044愿用专业的组学技术,和您一路前行!
参考文献:
[1] Chen D, Pan Y, Wang Y, et al. The chromosome-level reference genome of Coptis chinensis provides insights into genomic evolution and berberine biosynthesis[J]. Horticulture research, 2021, 8.
[2] Liu Y, Wang B, Shu S, et al. Analysis of the Coptis chinensis genome reveals the diversification of protoberberine-type alkaloids[J]. Nature communications, 2021, 12(1): 1-13.
[3] Yuan Y, Jin X, Liu J, et al. The Gastrodia elata genome provides insights into plant adaptation to heterotrophy[J]. Nature Communications, 2018, 9(1): 1-11.
[4] Xu Y, Lei Y, Su Z, et al. A chromosome‐scale Gastrodia elata genome and large‐scale comparative genomic analysis indicate convergent evolution by gene loss in mycoheterotrophic and parasitic plants[J]. The Plant Journal, 2021, 108(6): 1609-1623.
[5] Yin Y, Peng F, Zhou L, et al. The chromosome-scale genome of Magnolia officinalis provides insight into the evolutionary position of magnoliids[J]. Iscience, 2021, 24(9): 102997.
[6] Miao Y, Luo D, Zhao T, et al. Genome sequencing reveals chromosome fusion and extensive expansion of genes related to secondary metabolism in Artemisia argyi[J]. Plant Biotechnology Journal, 2022.
[7] Liu H, Wang X, Wang G, et al. The nearly complete genome of Ginkgo biloba illuminates gymnosperm evolution[J]. Nature Plants, 2021, 7(6): 748-756.
[8] Luo H, Qian J, Xu Z, et al. The Wolfiporia cocos genome and transcriptome shed light on the formation of its edible and medicinal sclerotium[J]. Genomics, proteomics & bioinformatics, 2020, 18(4): 455-467.
[9] Wang Q, Huang B, Liu D, et al. Genome Resequencing and Transcriptome Analysis Reveal the Genetic Diversity of Wolfiporia cocos Germplasm and Genes Related to High Yield[J]. Current Microbiology, 2022, 79(10): 1-14.
 微信公众号
微信公众号
