
近日,上海交通大学医学院附属仁济医院风湿病学研究所沈南教授团队在国际知名期刊Nature Communications(IF=12.121)上发表了题为“SLE non-coding Genetic Risk Variant Determines the Epigenetic Dysfunction of an Immune Cell Specific Enhancer that Controls Disease-critical microRNA Expression ”的研究成果。该研究通过表观遗传学、3D基因组学以及CRISPR技术,阐明了在狼疮发病关键通路中起重要调控作用的非编码RNA在特定免疫细胞亚群中异常表达的分子遗传学机制,为今后系统鉴定大量SLE非编码遗传因子的生物学功能及发展细胞特异性干预手段提供了新的研究范式。永利集团3044承担了RNA测序和4C数据挖掘工作。

图1 文章发表信息
研究思路
材料:U-937、Raji、Jurkat和HEK-293T细胞系、PBMC
技术:ATAC-seq、 RNA-seq、4C、ChIP、CRISPR
研究结果
1.SLE风险位点rs2431697的遗传和表观基因组分析
在之前研究中,miR-146a在SLE发病机制中发挥了重要作用,通过GWAS发现该ncRNA基因附近(PTTG1-MIR3142HG)有SLE风险关联信号。为了进一步精细定位,研究人员利用 discovery cohort和 replication cohort,通过 Gtrans-ancestral meta-analysis分析发现rs2431697与SLE存在关联。eQTL分析发现,rs2431697对miR-146a基因表达有影响。
通过MPRA筛选所有基因组范围内与SLE相关的重要遗传变异的等位基因增强子活性,发现rs2431697具有明显的基因型依赖性增强活性。基于公开表观遗传学数据分析,在CD14+单核细胞中rs2431697区域观察到了强H3K4me1和H3K27ac信号,CD19+B细胞中发现了H3K4me1修饰,而CD4+T细胞和CD8+T细胞中均未检测到信号。同时,ATAC-seq分析显示该染色质区域仅在CD14 +单核细胞中开放。这些结果表明包含rs2431697的区域可能是调节附近基因表达的细胞特异性增强子。
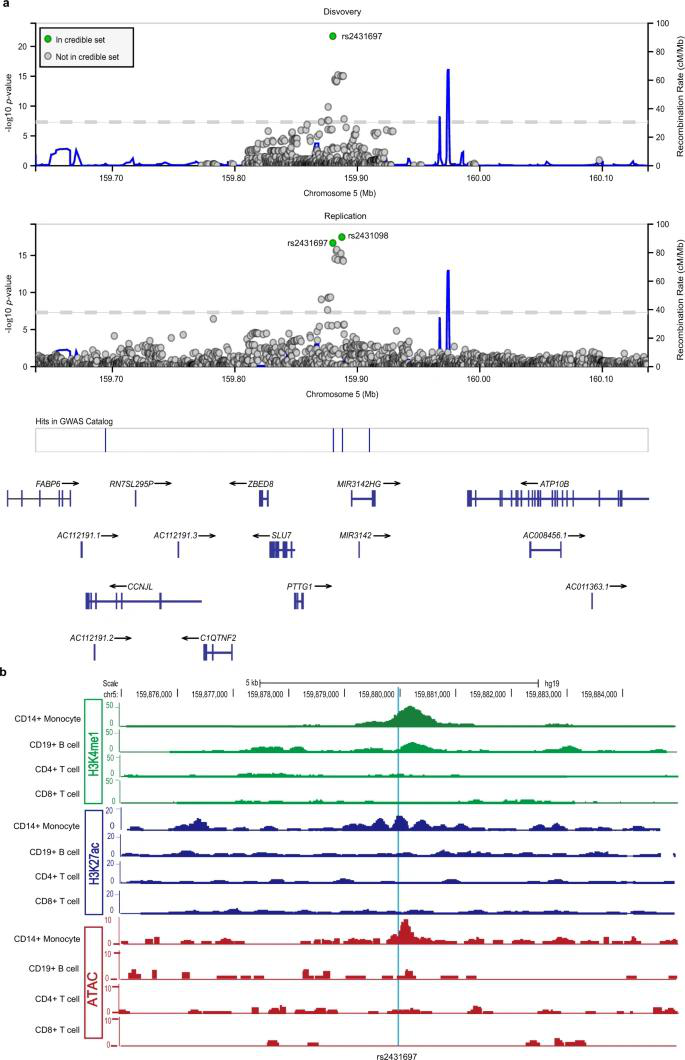
图1 SLE风险位点rs2431697的遗传和表观基因组分析
2.rs2431697区域特异性调节miR-146a表达
研究者对U-937细胞系中rs2431697基因座进行了CRISPRi和CRISPRa实验,分别导致miR-146a的显著提高和降低,而且rs2431697的2 Mb区域内附近基因的表达没有受到影响。为了直接评估包含rs2431697的区域在调控miR-146a表达中的作用 ,敲除U-937细胞系中的rs2431697的30 bp区域。与WT相比,在未刺激和TNFα刺激的条件下,敲除30 bp区域的U-937细胞中miR-146a的表达均较低,且miR-146a是在rs2431697的2 Mb区域内唯一受影响的基因,这些都表明rs2431697区域的功能增强子特异性调节miR-146a表达。

图2 rs2431697区域的功能增强子特异性调节miR-146a表达
为了验证rs2431697区域细胞特异性调节miR-146a表达,研究者敲除Raji和Jurkat细胞30bp区域。在Jurkat细胞中miR-146a表达没有显著变化,而Raji细胞与U-937细胞相似。在U-937和Raji细胞中,该区域具有高度富集的H3K4me1和H3K27ac信号, 而Jurkat细胞中,几乎没有增强子标记的信号,表明该调节元件的功能与观察到的表观遗传修饰一致。同时在不同免疫细胞类型中观察到的表观遗传学修饰一致,破坏rs2431697的区域会显着降低CD14+单核细胞中的miR-146a表达,而不会在CD3+T细胞或CD19+B细胞中降低。
将人类整个PBMC注射NSG小鼠来构建人性化的小鼠模型,使用miScript单细胞qPCR试剂盒,可在分离的细胞中定量miR-146a表达。包含rs2431697的基因组区域的破坏仅降低了单核细胞中miR-146a的表达。 总而言之,体外和体内数据表明,包含rs2431697的区域在体内具有功能性细胞特异性增强子,可调节miR-146a在人原代细胞中的表达。
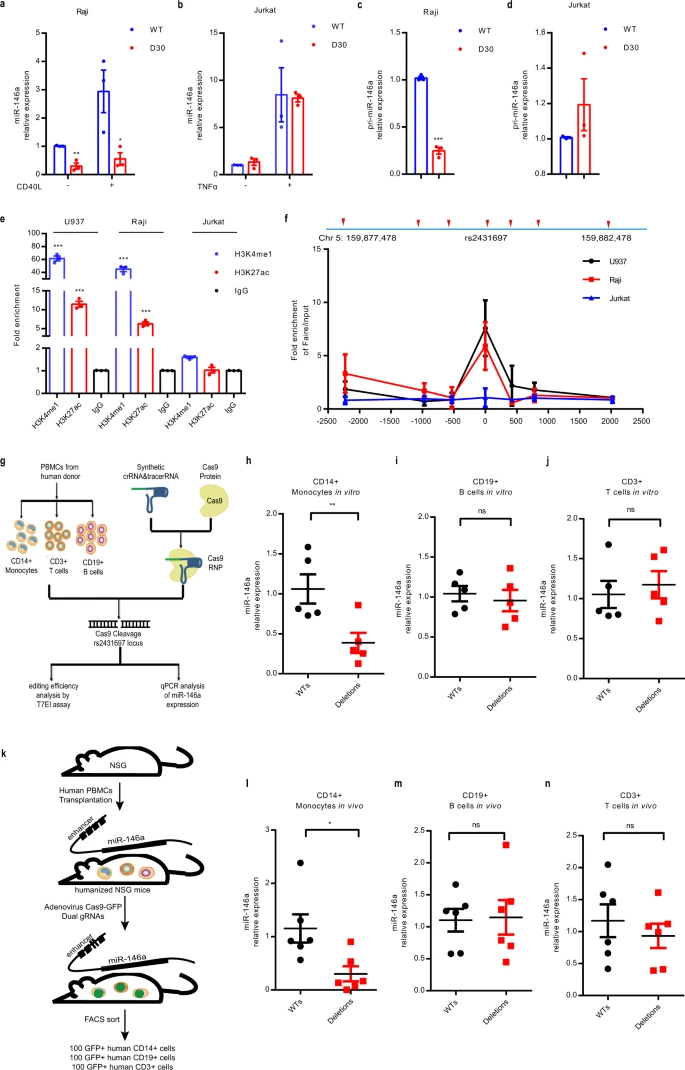
图3 体内外验证rs2431697区域细胞特异性调节miR-146a表达
3.rs2431697的调控元件与miR-146a启动子互作
远端增强子通常通过与靶基因启动子位点形成增强子-启动子loop环来影响基因表达,MIR3142HG编码miR-146a的基因具有两个启动子。一个远端启动子,包含一个PLZF结合位点 ,一个近端启动子,其中包含一个PLZF结合位点。利用CRISPR / Cas9技术分别敲除NF-KB结合位点序列和PLZF结合位点序列。NF-KB结合位点的缺失导致在未刺激和TNFα刺激条件下miR-146a表达均显着降低,然而PLZF结合位点的缺失并没有显着影响miR-146a的表达。环化染色体构象捕获测序(4C-seq)分析表明,rs2431697区域和miR-146a启动子区域存在互作。这表明远端启动子在U-937细胞中启动了MIR3142HG转录,从而导致miR-146a的后续表达。
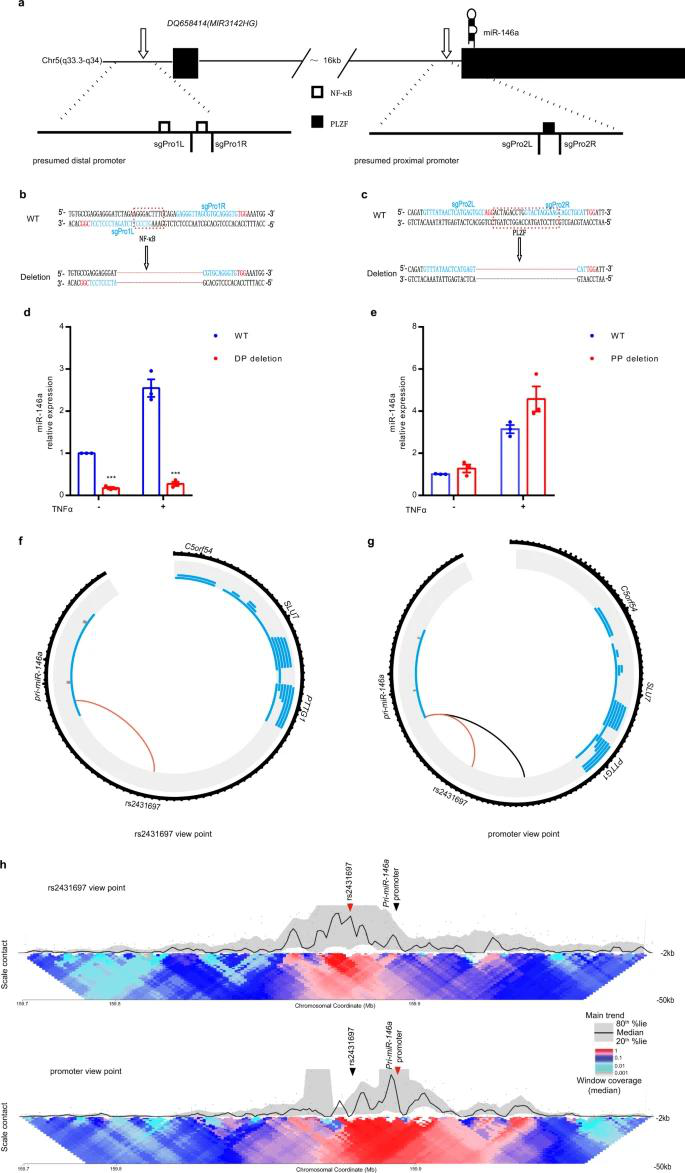
图4 rs2431697的调控元件与miR-146a启动子互作
调节区中的SNP通常通过影响转录因子(TF)结合而发挥作用,研究者通过ChIP-qPCR等技术,发现包含rs2431697 C非风险等位基因的DNA序列以更高的亲和力结合NF-KB,并且相对于rs2431697 T风险等位基因具有更高的可及性,从而驱动miR-146a的表达增加,表明不同等位基因差异性影响转录因子的结合和染色体开放状态,精细调控狼疮致病基因的表达。
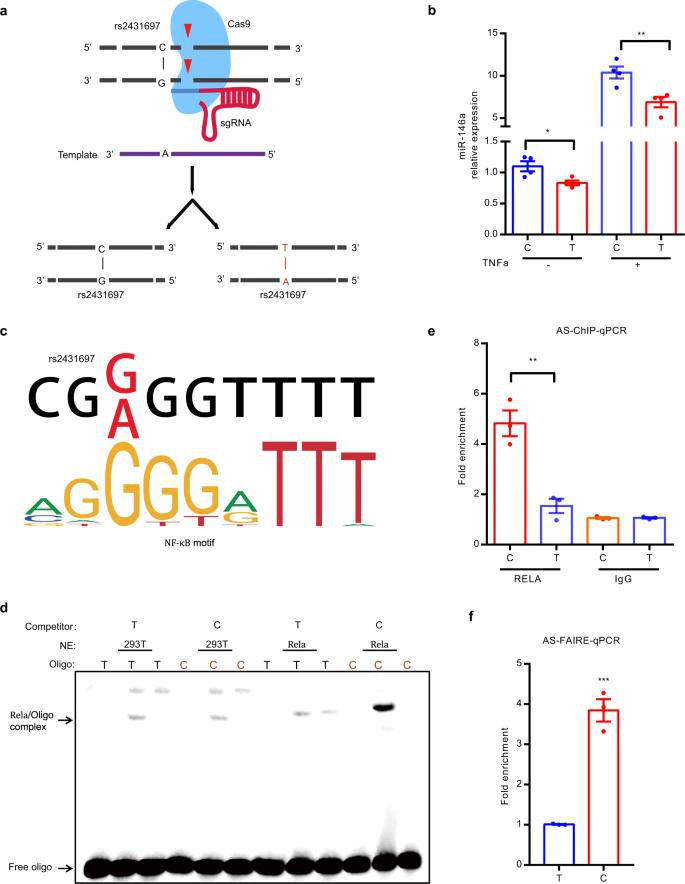
图5 SLE风险相关SNP rs2431697改变NF-KB结合和染色质状态以调节miR-146a表达
4.靶向rs2431697的增强子区域可通过上调miR-146a表达来减弱SLE IFN评分
作为I型干扰素途径的关键负调控因子,miR-146a在SLE中是有吸引力的治疗靶标,部含rs2431697的区域是miR-146a表达的关键调节因子,而SLE患者PBMC中miR-146a表达降低,提供了一种新的SLE治疗方法。使用了CRISPRa系统靶向rs2431697基因座,来激活miR-146a表达。
与WT相比,rs2431697区域缺失对干扰素α刺激更敏感,干扰素信号响应基因IFIT1,IFIT3,OAS1和IFI44的表达增加,表明SLE风险介导包含rs2431697的区域可能通过I型干扰素途径内的miR-146a靶基因调控发挥良好作用。接下来,研究者从具有高IFN评分的SLE患者中分离出PBMC,并在这些PBMC中进行了CRISPRa实验,pri-miR-146a表达上调,IFN评分降低。靶向作用于遗传易感位点所在的增强子来特异性升高单核细胞内miR-146a的水平,从而有效阻断狼疮病人干扰素通路的异常活化。
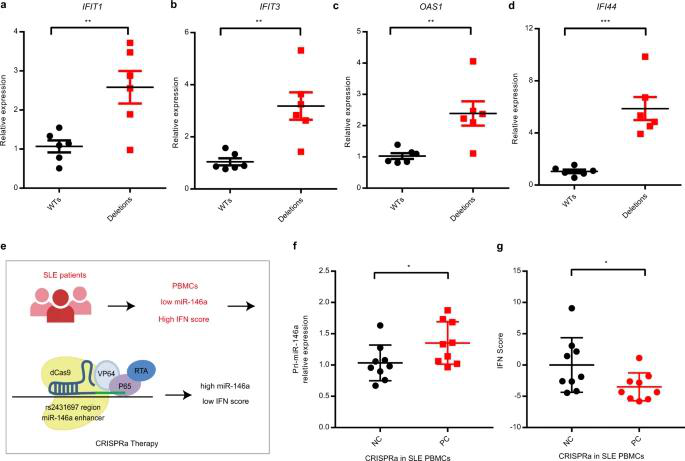
图6 靶向rs2431697调节miR-146a表达干预干扰素途径的激活
总结
本研究通过利用疾病风险SNP信息定位ncRNA调控元件,阐明了风险变异rs2431697在SLE发病机理中的功能机制,展示了一种筛选功能性疾病易感位点和功能性调控元件的策略,并将自身免疫性疾病风险遗传变异与自身免疫性疾病病因联系起来,为自身免疫性疾病的治疗提供了新的方向和靶点。
上海交通大学医学院仁济医院沈南教授为本文通讯作者,仁济医院侯国俊博士和美国辛辛那提儿童医学中心Isaac T.W. Harley博士为本文共同第一作者。这项工作得到国家自然科学基金,国家人类遗传资源共享服务平台,上海市重点医学中心建设项目的支持。
参考文献:
Hou G, Harley I T W, Lu X, et al. SLE non-coding genetic risk variant determines the epigenetic dysfunction of an immune cell specific enhancer that controls disease-critical microRNA expression[J]. Nature communications, 2021, 12(1): 1-19.
 微信公众号
微信公众号
