
说到癌症,不得不提到其中的“头号杀手”---肺癌。肺癌是发病率和死亡率增长最快,对人群健康和生命威胁最大的恶性肿瘤之一。近50年来许多国家都报道肺癌的发病率和死亡率均明显增高,男性肺癌发病率和死亡率均占所有恶性肿瘤的第一位,女性肺癌发病率和死亡率占第二位。由于肺癌患者基数之大,使得众多科研工作者和医务人员进入这一领域,带来了全球的学术热潮。近年来,随着单细胞测序技术的蓬勃发展,肺癌单细胞测序文章数量也位列众多癌种榜首。本文归纳总结10篇经典肺癌单细胞文章,全面了解肺癌单细胞测序研究思路,希望能为大家的肿瘤单细胞研究提供一定的参考。
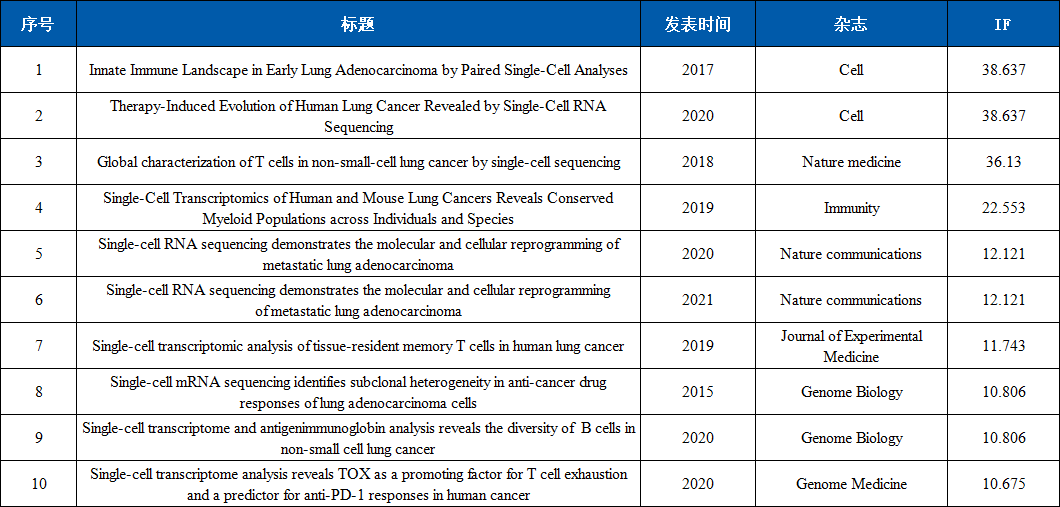
表1 十篇经典肺癌单细胞测序文章基本信息
01

标题:配对的单细胞分析揭示早期肺癌的先天免疫景观
样本:32位NSCLS患者的肿瘤组织、正常组织以及外周血
测序方案:TCRβ CDR3-seq、massively parallel single cell RNA-Seq (MARS-Seq)
主要结果:为了指导早期肺肿瘤患者免疫治疗策略的设计,研究人员开发了一种多尺度免疫图谱策略来绘制早期肺腺癌病变的免疫景观,以寻找肿瘤驱动的免疫变化。利用条形码方法,可以同时对肿瘤到、正常组织和血细胞进行单细胞分析,提供了早期肺肿瘤详细的免疫细胞图谱。发现I期肺腺癌病变已经包含明显改变的T细胞和NK细胞隔间。此外,还发现了肿瘤浸润髓细胞(TIM)亚群的变化可能会损害抗肿瘤T细胞免疫。因此,配对样本的单细胞分析为肿瘤驱动的免疫变化提供了有价值的信息,为合理设计免疫治疗提供了强有力的工具。
02
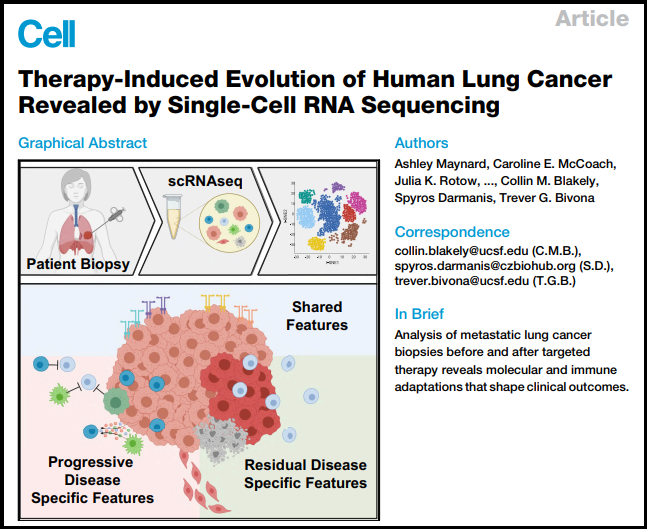
标题:单细胞RNA测序揭示肺癌治疗诱导的进化
样本:30名肺癌患者的49个样本,包括45个肺腺癌、1个鳞状细胞癌和3个肿瘤邻近组织
测序方案:Smart-Seq2
主要结果:该研究对来自30个病人的靶向治疗前后的49个临床活检样本做了单细胞RNA-seq测序。超过20000个癌症和肿瘤微环境(TME)的单细胞图谱暴露了丰富而动态的肿瘤生态系统,癌细胞的scRNA-seq揭示了临床上检测不到的可靶向癌基因。作为治疗后存活的残余病灶(RD),癌细胞表达了肺泡-再生细胞的特征,表明治疗诱导的原始细胞状态的转变,而那些存在于治疗中的进展性疾病(PD)的癌细胞则上调了犬尿氨酸、质粒原和间隙连接通路。研究人员还发现,RD时存在活跃的T淋巴细胞和减少的巨噬细胞,PD时存在免疫抑制细胞状态的特征。scRNA-seq揭示的生物学特征是独立队列中临床结果的生物标志物。这项研究强调了治疗诱导的转移性癌症多细胞生态系统的适应性如何导致肺癌的临床结果。
03

标题:非小细胞肺癌中T细胞的单细胞测序研究
样本:14例非小细胞肺癌的患者,包括11例腺癌和3例鳞状细胞癌患者
测序方案:Smart-Seq2、TraCeR方法分析组装TCR CDR3序列
主要结果:研究人员对来自14个药物治疗前非小细胞肺癌患者的外周血、癌旁组织和癌组织的12,346个T细胞进行了单细胞转录组测序。基于T细胞的转录组数据及T细胞受体(TCR)序列,通过生物信息学手段分析细胞的亚群分类、组织分布特征、肿瘤内群体异质性及药物靶基因表达情况,该研究鉴定了跨组织分布的T细胞类群、肿瘤浸润T细胞的组成及亚群间潜在的状态转换关系,提出了新的肺腺癌临床标志物,也为免疫治疗特异性地靶向T细胞亚群提供了新的思路。
04
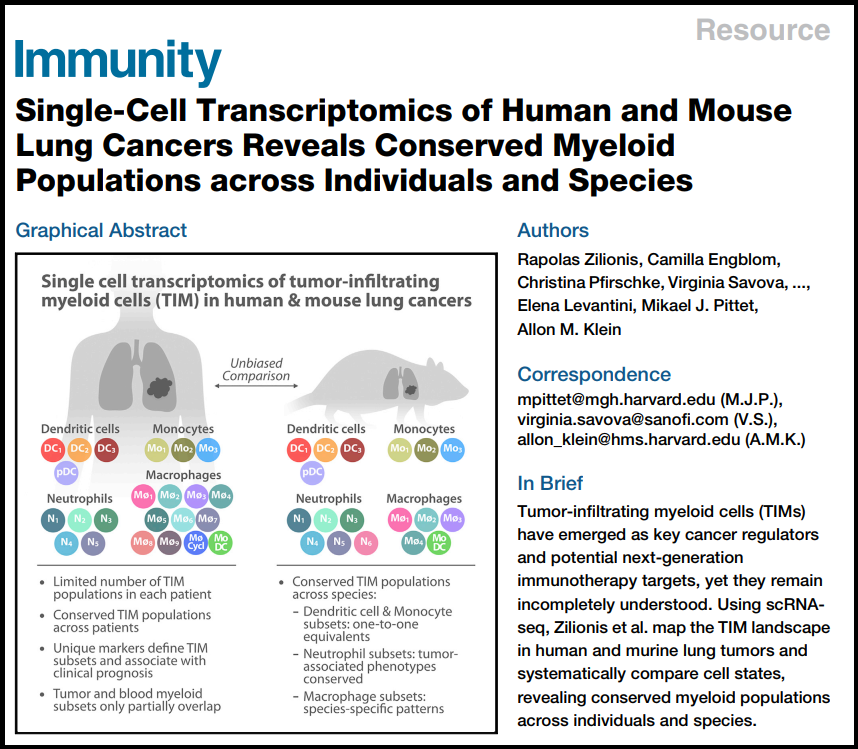
标题:人类和小鼠的肺癌单细胞转录组测序揭示肿瘤浸润髓系细胞跨越个体和物种的种群
样本:7例非小细胞肺癌的患者癌组织以及外周血、小鼠肺肿瘤组织
测序方案:Single-cell RNA-seq(BD)
主要结果:肿瘤浸润髓样细胞(TIMs)由单核细胞、巨噬细胞、树突状细胞和中性粒细胞组成,并已成为癌症生长的关键调控因子。这些细胞可以分化成多种状态,这些状态可能促进或限制肿瘤的生长,但对它们的了解仍很有限。本研究使用单细胞RNA测序(scRNA-seq)来绘制非小细胞肺癌患者的TIMs。发现了25个TIM群体,其中大多数可在患者中重复发现。为了促进这些群体的转译研究,还在小鼠中分析了TIMs。在比较不同物种的TIMs时,发现树突状细胞和单核细胞之间的种群结构几乎完全一致;保守的嗜中性粒细胞子集;巨噬细胞之间的物种差异。相比之下,患者血液中的髓细胞群结构与TIMs有有限的重叠。本研究确定了肺TIM的景观,并为将来研究TIM作为免疫治疗靶点的潜力奠定了基础。
05

标题:晚期非小细胞肺癌肿瘤异质性和微环境的单细胞图谱
样本:42例肺癌患者,包括18例肺腺癌、18例鳞状肺癌和6例非小细胞肺癌三种类型的35例治疗前癌组织、2例TKI治疗失败后癌组织、3例免疫治疗失败后癌组织,2例化疗失败后癌组织
测序方案:Single-cell RNA-seq (Singleron)
主要结果:该研究分析了42例III / IV 期NSCLC患者癌组织样本。除了之前关于早期肺癌的单细胞研究中描述的细胞类型,还鉴定到了肿瘤中罕见的细胞类型,如滤泡树突状细胞和T辅助17细胞。不同患者的肿瘤在细胞组成、染色体结构、发育轨迹、细胞间信号网络和表型优势等方面表现出较大的异质性。该研究还揭示了肿瘤异质性与肿瘤相关中性粒细胞的相关性,这可能有助于阐明它们在非小细胞肺癌中的功能。
06

标题:单细胞RNA测序显示转移性肺腺癌的分子和细胞重编程
样本:44例LUAD患者、肿瘤组织、远端正常肺、正常淋巴结以及转移性脑组织;另外收集3例LUAD患者的肿瘤以及配对正常组织
测序方案:10× single-cell RNA-seq、WES
主要结果:晚期转移性癌症带来最大的临床挑战,可能呈现不同于早期癌症的分子和细胞特征。研究人员利用单细胞转录组分析在44例患者中,从正常组织或早期到转移阶段的208,506个细胞中,确定了一种偏离正常分化轨道并主导转移阶段的癌细胞亚型。在所有阶段,基质细胞和免疫细胞动力学揭示了本体和功能的变化,创造了一个前肿瘤和免疫抑制微环境。随着T细胞衰竭,正常的骨髓细胞群逐渐被单核来源的巨噬细胞和树突状细胞所取代。这种广泛的单细胞分析增强了对转移性肺癌分子和细胞动力学的理解,并揭示了癌症-微环境相互作用中潜在的诊断和治疗靶点。
07

标题:肺癌组织驻留记忆T细胞的单细胞转录组分析
样本:12个肺癌患者的肿瘤组织和6个配对的正常组织
测序方案:Bulk RNA-seq 、TCR-seq、10× single-cell RNA-seq
主要结果:大量的组织驻留记忆T (TRM)细胞与癌症患者更好的临床结果相关。然而,驱动它们对肿瘤产生有效免疫反应的分子特征尚不清楚。本研究利用单细胞转录组以及Bulk转录组分析肿瘤和正常肺组织的TRM和 non-TRM细胞。结果表明,与表达PD-1的非TRM细胞相比,肿瘤中表达PD-1的TRM细胞可以克隆扩增并富集与细胞增殖和细胞毒性相关的转录本。这一特征在共同表达PD-1和TIM-3的TRM细胞亚群中更为突出,并且在体外功能分析中得到了验证,也反映在它们的染色质可及性谱上。这种PD-1+TIM-3+ TRM细胞亚群在PD-1抑制剂应答者和具有更大程度细胞毒性T细胞(CTL)响应的肿瘤中富集。这些数据强调并不是所有表达PD-1的CTL都是功能失调的;相反,表达PD-1的TRM细胞具有更优越的功能。
08

标题:单细胞转录组测序发现肺腺癌细胞抗肿瘤药物反应的亚克隆异质性
样本:小鼠移植瘤PDX细胞
测序方案:WES、单细胞RNA测序采用 C1™ Single-Cell Auto Prep System C1 array chip
主要结果:研究人员分离了34个异种移植(PDX)肿瘤细胞,对单个肿瘤细胞进行单细胞RNA-seq基因表达谱和表达突变谱分析。在单个PDX细胞中观察到50种肿瘤特异性的单核苷酸变异,包括KRASG12D。基于KRASG12D突变表达和代表69个肺腺癌预后基因表达的风险评分,将PDX细胞分为4组。体外抗肿瘤药物治疗后存活的PDX细胞表现出与KRASG12D和低风险评分组特征一致的转录组特征。结果显示,活PDX细胞上的单细胞RNA-seq鉴定出了一个与抗癌耐药相关的候选肿瘤细胞亚群。因此,单细胞RNA-seq是一种识别独特肿瘤细胞特异性基因表达谱的有力方法,这将有助于优化临床抗癌策略的制定。
09

标题:单细胞转录组和抗原免疫球蛋白分析揭示了非小细胞肺癌中B细胞的多样性
样本:11例NSCLC肿瘤组织,包括6例stage-I和5例stage-III
测序方案:10 × single-cell RNA-seq
主要结果:研究人员对非小细胞肺(NSCLC)患者肿瘤组织样本中分离的细胞进行了单细胞RNA-seq分析,确定了肿瘤浸润B细胞的亚型及其在NSCLC进展中的多种功能。流式细胞术和免疫组化实验两组独立队列证实了B细胞的两种主要亚型naïve-like和plasma-like B细胞共存。在晚期NSCLC中naïve-like B细胞减少,其水平较低与预后不良相关。从NSCLC患者中分离的naïve-like B细胞与两种肺癌细胞系共培养,结果显示naïve-like B细胞通过分泌4种负调控细胞生长的因子抑制肺癌细胞的生长。同时还发现,血浆样B细胞在NSCLC早期抑制癌细胞生长,但在NSCLC晚期促进细胞生长。蛋白组学数据进一步证实了plasma-like B细胞产生的免疫球蛋白及其相互作用蛋白在NSCLC进展中的作用。结果揭示了肿瘤浸润B细胞的多种功能及其在非小细胞肺癌中的潜在临床意义。
10

标题:单细胞转录组分析揭示人类癌症中TOX作为T细胞衰竭的促进因子和抗PD-1反应的预测因子
公共数据库数据挖掘分析样本: 17例黑色素瘤患者肿瘤样本的单细胞转录组数据(GSE72056)和14例NSCLC患者单细胞转录组数据(GSE99254)
主要结果:
研究人员分析了人类黑色素瘤和NSCLC中肿瘤浸润(TI) CD8+ T细胞中PDCD1(PD-1)-high亚群和PDCD1-low亚群差异表达基因中调节T细胞衰竭的许多已知因素。TOX是唯一预测两种肿瘤类型的转录因子(TF)。当CD8+ T细胞被耗尽时,TOX水平趋于增加。流式细胞术分析显示TOX表达与肿瘤内T细胞衰竭的严重程度相关。在人肿瘤浸润 CD8+ T细胞中,TOX敲低导致PD-1、TIM-3、TIGIT和CTLA-4下调,这表明TOX通过上调癌症中的免疫检查点蛋白促进肿瘤内T细胞衰竭。最后,肿瘤浸润T细胞中的TOX水平被发现能够高度预测黑色素瘤和NSCLC患者的总生存期和抗PD-1疗效。
总 结
综上所述,关于肺癌不同平台的单细胞测序的研究主要关注在以下几个方面 :
(1)不同肺癌类型、不同分期以及转移之间的异质性研究;
(2)免疫微环境中不同细胞类型的研究;
(3)靶向治疗、免疫治疗有效性的研究;
(4)以PDX模型为样本或者基于公共数据库数据与其他癌种比较的研究;
(5)结合其它组学肿瘤的异质性研究。
基于此,其它类型肿瘤单细胞测序工作的开展需避开本癌种已有的研究思路,然后借鉴肺癌单细胞研究套路设计类似方案,发现新的生物学问题。
参考文献:
[1] Lavin Y, Kobayashi S, Leader A et al. 2017. Innate Immune Landscape in Early Lung Adenocarcinoma by Paired Single-Cell Analyses. Cell 169, 750-765.
[2] Maynard A, McCoach CE, Rotow JK et al. 2020. Therapy-Induced Evolution of Human Lung Cancer Revealed by Single-Cell RNA Sequencing. Cell 182, 1232-1251.
[3] Guo XY, Zhang YY, Zheng LT et al. 2018. Global characterization of T cells in non-small-cell lung cancer by single-cell sequencing. Nature Medicine 24, 978-985.
[4] Zilionis R, Engblom C, Pfirschke C et al. 2019. Single-Cell Transcriptomics of Human and Mouse Lung Cancers Reveals Conserved Myeloid Populations across Individuals and Species. Immunity 50, 1317-1334.
[5] Wu FY, Fan J, He YY et al. 2021. Single-cell profiling of tumor heterogeneity and the microenvironment in advanced non-small cell lung cancer. Nature communications 12, 2540.
[6] Kim N, Kim HK, Lee KJ et al. 2020. Single-cell RNA sequencing demonstrates the molecular and cellular reprogramming of metastatic lung adenocarcinoma. Nature communications 11, 2285.
[7] Clarke J, Panwar B, Madrigal A et al. 2019. Single-cell transcriptomic analysis of tissue-resident memory T cells in human lung cancer. J Exp Med 216 (9), 2128-2149.
[8] Kim KT, Lee HW, Lee HO et al. 2015. Single-cell mRNA sequencing identifies subclonal heterogeneity in anti-cancer drug responses of lung adenocarcinoma cells. Genome Biology 16, 127.
[9] Chen J, Tan Y, Sun FH et al. 2020. Single-cell transcriptome and antigenimmunoglobin analysis reveals the diversity of B cells in non-small cell lung cancer. Genome Biology 21, 152.
[10] Kim KS, Park S, Park SY et al. 2020. Single-cell transcriptome analysis reveals TOX as a promoting factor for T cell exhaustion and a predictor for anti-PD-1 responses in human cancer. Genome Medicine 12, 22.
 微信公众号
微信公众号
