
新冠病毒SARS-CoV-2是最大的单股正链RNA病毒之一,由它引起的COVID-19新冠肺炎已在全球造成数百万人死亡,相关的研究进展和疫苗研发是世界性议题。SARS-CoV-2可以连续复制合成基因组RNA(gRNA),还能以非连续转录的方式产生亚基因组mRNA(sgRNA或sgmRNA),其转录过程受到位于前导序列3' 末端的转录调节序列 (TRS-L)和每个病毒基因前的转录调节序列(TRS-B) 的控制,并且TRS-L核心序列(CS-L)需与每一个CS-B的新生互补负链(cCS-B)形成碱基配对。尽管人们普遍认为TRS-L与cCS-B存在相互作用,但并没有其直接相互作用的实验证据。RNA的二级结构对于病毒的复制、转录、翻译具有重要作用,且远距离的RNA互作被认为对于形成高级结构促进非连续RNA的合成也具有重要作用,然而已有的SARS-CoV-2的 RNA-RNA互作研究是在病毒生命周期中的某一特定时期进行的,对于病毒整个生命周期内的RNA结构动态变化及其功能相关性仍不清楚。
由军事科学院军事医学研究院赵志虎研究组主导,联合华中农业大学金梅林研究组、英国爱丁堡大学Grzegorz Kudla组和武汉永利集团3044等团队合作完成的新冠病毒RNA结构研究成果于2021年9月28日以题为“In vivo structure and dynamics of the SARS-CoV-2 RNA genome”发表于国际著名期刊Nature Communications。研究者使用简化版SPLASH方法,全面绘制了SARS-CoV-2在整个生命周期的体内RNA-RNA相互作用,提供了转录调节序列(TRS-L 和 TRS-Bs)之间相互作用的第一个直接证据,发现其基因组 RNA 经历了强烈的压缩,但基因组结构域保持稳定,结构域特征信号增强,全局环化减弱。该研究为病毒复制、不连续转录和翻译移码的调节提供了结构基础,描述了SARS-CoV-2生命周期中RNA结构的动态变化,将有助于人们开发出更好的抗病毒策略。
永利集团3044在本研究中承担了部分RNA-RNA互作数据分析工作。

巧合的是,在刚刚结束的第九届武汉现代病毒学国际研讨会上(2021年9月26~28日),文章通讯作者之一赵志虎研究员于2021年9月28日下午在会上就此工作做了专题报告,当天晚上,文章见刊于Nature Communications。

第九届武汉现代病毒学国际研讨会,赵志虎研究员专题报告(2021年9月28日)
研究结果
1.SARS-Cov-2的RNA-RNA相互作用、UTR结构和基因组环化
在感染的早期阶段,研究者收集病毒感染的Vero细胞 (C),此时未观察到细胞病变效应(CPE)。在后期,当70%的细胞出现CPE时,研究者收集细胞培养上清液并收集成熟病毒颗粒(V),同时裂解细胞(L)以收集细胞和病毒RNA,随后通过简化SPLASH方法捕获这些阶段的SARS-CoV-2中的RNA-RNA相互作用。
研究者鉴定出了对于冠状病毒复制和不连续转录至关重要的5'-UTR的全部五个保守茎环结构(SL1-SL5),并且在3' stem-loop II-like motif (S2M)区域鉴别到一个替代的3'-UTR结构。在互作矩阵中,研究者发现了SARS-CoV-2基因组5'-end和3'-end之间的相互作用,确定了基因组环化(genome cyclization)现象并推测其与复制/包装有关。
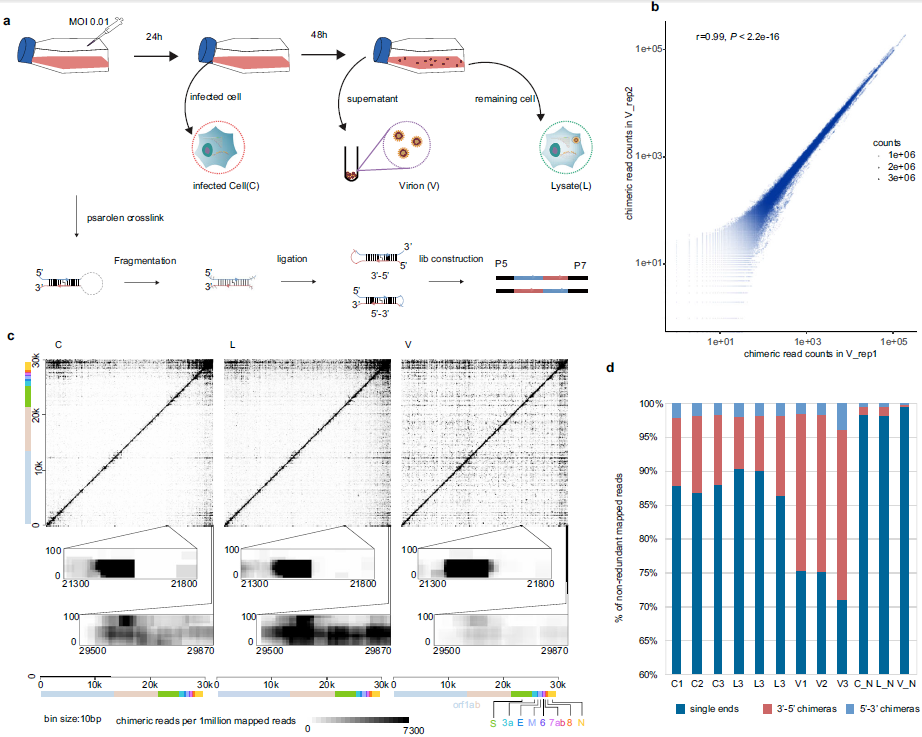
图1 实验设计和不同感染阶段SARS-CoV-2的RNA互作图谱
2.TRS-L和TRS-B区域之间的远程相互作用以及鉴定和验证新的依赖TRS-L的sgRNA
RNA邻近连接反应能得到RNA-RNA相互作用信息,其中包含一部分剪切本之间的连接,也包含sgRNA自身及其与宿主RNA因空间邻近而连接的嵌合分子。为了正确识别RNA-RNA相互作用,研究者评估了已发布的SARS-CoV-2感染细胞RNA-Seq数据集,确定了三个特征来将RNA-Seq中发现的大多数sgRNA嵌合体与真正的邻近连接嵌合体区分开来:
sgRNAs几乎完全以5'-3'方向连接,而RNA邻近连接嵌合体可以为5'-3'方向和3'-5'方向;
嵌合体臂之间的连接点精确定位在sgRNAs中,而邻近连接中的连接位点是可变的;
sgRNA嵌合体通常包括嵌合体的TRS-L和TRS-B侧之间的同源区域 ,而邻近连接嵌合体通常不包括这样的区域。
研究者通过调整分析流程参数可以检测或去除RNA-Seq数据中大多数sgRNA嵌合体,使用严谨参数流程来分析邻近连接数据,同时过滤掉sgRNA。通过分析5'-3'和 3 '-5'嵌合体以识别由TRS-L介导的RNA-RNA相互作用,并分析TRS-L连接位点的分布,发现可以区分实验数据中TRS-L介导的RNA-RNA相互作用和TRS-L依赖的sgRNA。远程相互作用介导的RNA碱基配对表明TRS-L可能与TRS-B区域稳定结合。有趣的是, TRS-L通常不与确切的TRS-B序列相互作用,而是与50nt内的侧翼序列相互作用,这可能是为下一步配对Ccs-B和模板转换提供灵活性。
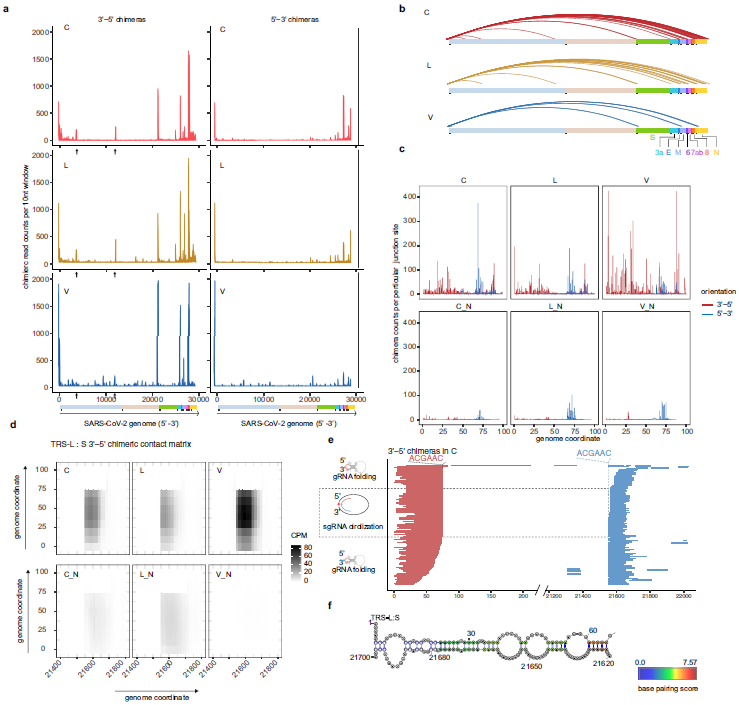
图2 TRS-L与经典TRS-B位点的互作
3.移码元件附近的多样结构
冠状病毒的一个特征是使用程序化的核糖体移码来促进ORF1b编码RdRp的翻译并控制其蛋白质的相对表达。研究者分析了移码元件(FSE)的相互作用,不仅发现了之前已经报道的三茎假结结构,还发现了更大的嵌有FSE的稳定茎环(arch1)的可选择局部结构,以及多种由FSE介导的远程相互作用,并鉴定得到多个强远程互作,利用三维建模对其进行了可视化。
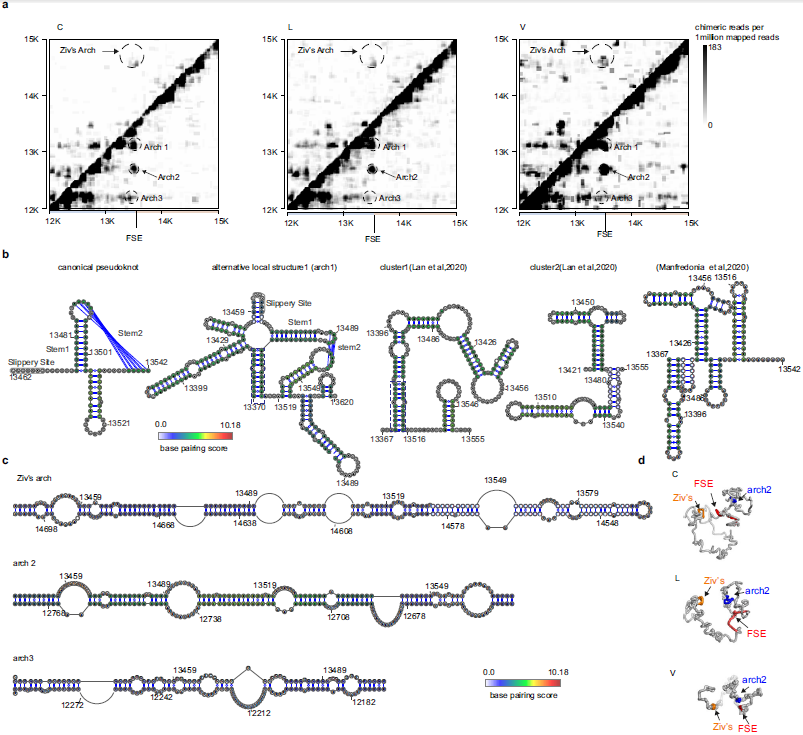
图3 局部可变及远程的FSE结构
4.SARS-CoV-2生命周期中RNA结构的动态变化
研究者通过相关性分析、主成分分析和差异分析展示了病毒生命周期各个阶段的互作动态,结果表明,与细胞组和裂解组相比,病毒衣壳中SARS-CoV-2基因组的三分之一的相互作用密度较低、基因组环化减少,然而病毒粒子和裂解细胞中近端和长程相互作用在增加,意味着基因组在包装成病毒粒子期间发生压缩,TRS-L区域介导的相互作用的变化则可能反映了病毒基因组包装的第一步。研究者还发现,病毒粒子长距离loop的差异互作中,减弱的相互作用几乎总是由sgRNA介导,而L组较C组也出现这种现象,表明RNA相互作用和构象在病毒包装过程中逐渐发生变化,sgRNAs丰度可能在减少。
简化的SPLASH数据热图类似于哺乳动物基因组Hi-C数据 ,研究者应用insulation score算法检查SARS-CoV-2基因组RNA是否被划分为domain,以及基因组RNA的整体压缩是否会导致domain的破坏,结果发现在基因组压缩和包装期间,domain结构不仅保留了,而且还得到了加强。最后,研究者通过计算SARS-CoV-2基因组的Shannon entropy value发现,细胞组比病毒粒子中的RNA有更灵活的结构,结构域边界的灵活性,可能是更有吸引力的药物设计靶点。
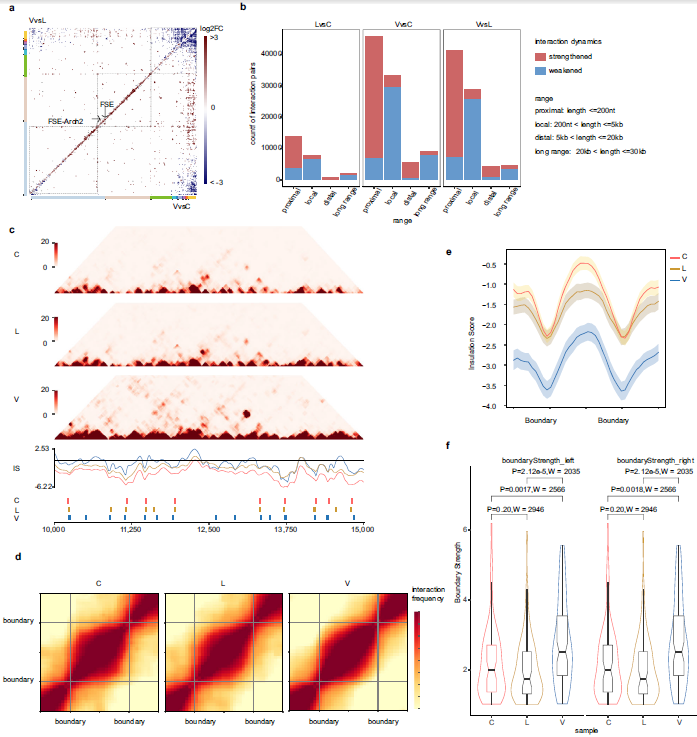
图4 SARS-CoV-2生命周期不同阶段的RNA互作动态
总 结
该研究简化了SPLASH方法,捕获了多个阶段的SARS-CoV-2中RNA-RNA相互作用,观察到了RNA经典和替代结构,包括 5'-UTR 和 3'-UTR、移码元件 (FSE) 假结和基因组环化,揭示了FSE附近的短距离和长距离arch形成嵌入FSE的“高阶假结”, 描述了SARS-CoV-2生命周期中RNA结构的动态变化,为其复制、不连续转录和翻译移码的调节提供了结构基础,将有助于人们开发出更好的抗病毒策略。
军事医学研究院张彦、华中农业大学黄坤、武汉永利集团3044谢德健为该论文的共同第一作者,军事医学研究院赵志虎研究员、华中农业大学金梅林教授、英国爱丁堡大学Grzegorz Kudla研究员为共同通讯作者。本研究得到了国家科技重大项目和国家重点研发计划的资助。
 微信公众号
微信公众号
