
众所周知,单细胞转录组测序中,悬液制备这一环节至关重要。10x Genomics单细胞实验需要载入活细胞悬液,对于细胞质量要求非常高,减少细胞结团、死细胞数、非细胞核酸(游离核酸)和潜在的逆转录抑制剂可获得高质量的数据,而且单细胞悬液制备的质量直接影响后续细胞捕获数,建库以及下机数据质量。单细胞悬液需要从细胞活性、结团率、细胞浓度等多个指标进行质检和评估,那么这些指标的意义是什么?解决方案是什么?小编来帮您详细梳理~
01
单细胞悬液10x上机标准及风险
细胞活性>90%
细胞活率低:油包水过程对活细胞、死细胞、碎片和颗粒等没有选择性,都会随机包裹,影响最终的结果:细胞数不准确、UMI分布曲线上有效细胞与非细胞界线不明显、线粒体基因过多等;
结团率<5%
结团率高:导致结在一起的两个或多个细胞被包在一个油包水中,被系统认为是一个细胞。结团率太高影响最终分析结果的准确性、过大的结团可能会堵芯片,导致实验彻底失败。
细胞浓度范围700-1200cells/μl
活细胞浓度不适宜:如活细胞浓度太低,但细胞总量足够时,可以进行浓缩,但是浓缩过程会造成细胞总量的损失、给细胞造成伤害、可能也会改变各细胞类型的比例;细胞浓度过高时,超过计数仪的分辨能力,导致计数不准确、结团率虚高、且过高的浓度易导致操作误差。
有核率>70%
有核率低:油包水过程对活细胞、死细胞、 碎片、颗粒和红细胞等没有选择性,都会被随机包裹,影响最终的结果,可能引起有效细胞识别不准确、有效细胞-非细胞界限模糊、背景升高等不利现象,有核率评估一定程度上可以预判这些问题。
细胞直径范围5-40μm
细胞直径:细胞直径太小时,超过细胞计数仪可识别的低限,会导致计数不准确, 最终细胞数误差较大;细胞直径太大, 会影响油包水结构的正常形成,可能导致实验失败。
02
单细胞悬液检测原理及结果判定
荧光检测活性检测原理
荧光染料AO:进入细胞膜
荧光染料PI :进入细胞膜和核膜 活细胞:AO、PI 绿光
死细胞(只有细胞核):PI 红光
计算发光比例:绿/红= 4% / 96%

图1 荧光场图
有核率=(FL1+FL2)/明场*100%

图2 明场图用来评估有核率
细胞直径分布符合正态分布
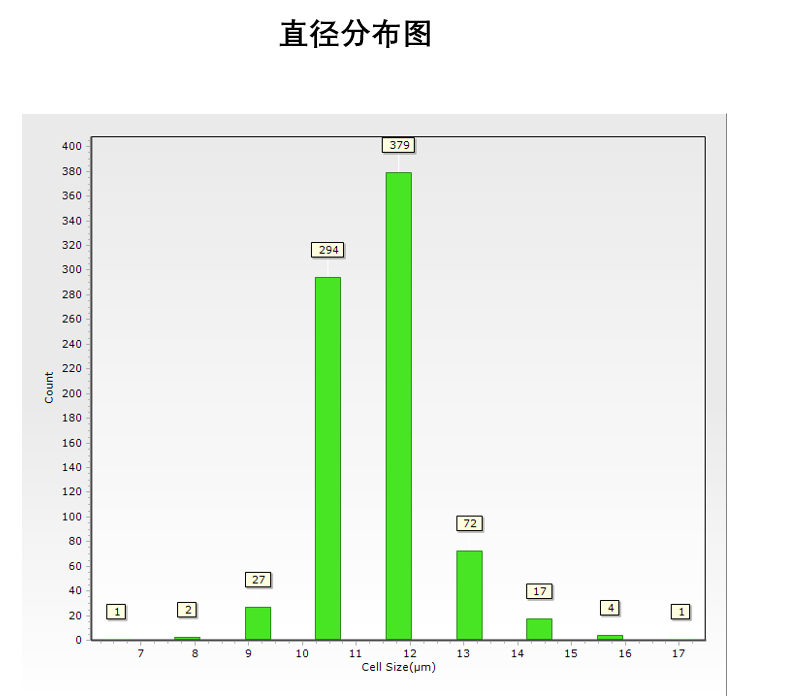
图3 直径分布图
03
不合格悬液优化方案推荐
活性低
当细胞活率<80%时,采用 10×Genomics推荐的MACS® Dead Cell Removal Kit(Miltenyi Biotec)(Order no: 130-090-101)对低活性的单细胞悬液进行去除死细胞操作。注意,去死细胞会造成一定量细胞损失。
杂质多
过筛处理:杂质较大时,可以选择过40μm或者30μm细胞筛进行过筛处理。(注意:需要去死细胞处理可不过细胞筛)。
去碎片处理:一般用于脑和成年小鼠心脏,杂质较多且较轻时,可以选择去碎片处理;杂质较重时无法去碎片;此外,需去碎片时尽量放在裂红前。
结团率高
导致结团率高的原因主要有组织消化不完全或细胞释放的DNA导致细胞黏连,因此在样本制备和细胞悬液清洗、重悬时增加部分操作针,降低细胞结团率。针对不同情况有以下处理方法:
组织解离时增加DNase;
提高细胞悬浮液BSA浓度;
细胞最后一次离心重悬移液动作轻柔,利用剪切力破坏细胞结团;
上机捕获细胞前,选择合适的细胞过滤器过滤细胞悬液。
有核率低
有核率偏低可能是单细胞悬液中碎片、颗粒等杂质较多或者裂红不彻底导致的,如何优化需具体问题具体分析。例如,提PBMC时吸到血小板后无法完全去除;小于正常细胞直径的间质碎片无法完全去除。
总 结
细胞优化均会损失细胞量,细胞活率太差(<30%)时,去死细胞后,虽细胞活率提升至90%以上,但大部分细胞都死了,细胞类型及分群会改变。
最后,请老师在准备阶段,一定要和我们的相关人员确认好每一步的准备注意事项,因为样本准备这一步是文库质量好坏的决定性因素。以上就是我们本次的单细胞悬液制备秘籍心得啦,小伙伴们有没有觉得收获满满?接下来单细胞团队的小伙伴们还会为大家带来更多单细胞方面的知识干货,让我们一起期待吧!
 微信公众号
微信公众号
