
POGZ是神经发育障碍和神经精神疾病患者中最经常发生突变的基因之一,包括引发精神分裂症、神经外胚层衍生的智力障碍和自闭症谱系障碍等疾病。然而,由POGZ突变引起的神经发育紊乱的潜在病因仍然难以确定。人们对其在胚胎干细胞(ESCs)、神经发育和疾病中的作用知之甚少。
近日,中国科学院水生生物研究所孙玉华研究团队在医学Top期刊Molecular Autism以“Autism-associated protein POGZ controls ESCs and ESC neural induction by association with esBAF”为题发表了相关研究。该研究表明,在胚胎干细胞向神经命运分化的过程中,POGZ是维持ESC特性和上调神经基因表达的必要条件。全基因组水平的结合分析表明,POGZ主要定位在基因启动子和增强子区域,其缺失会导致分化基因包括神经基因的失调。在ESC神经诱导过程中,POGZ介导esBAF/BRG1的招募和H3K27ac信号对于神经祖细胞基因的正常表达至关重要。
永利集团3044承担了该研究中Flag-POGZ蛋白的CUT&Tag建库测序及部分数据分析工作。

图1 文章信息
材料方法
研究材料:小鼠胚胎干细胞(mESC)
组学技术:RNA-seq、CUT&Tag、ChIP-seq、ATAC-seq
研究结果
1.POGZ影响ESC特性,在ESC神经诱导过程中助力神经祖基因表达
作者首先利用CRISPR/Cas9技术进行基因编辑,得到POGZ功能性无效的Pogz−/− ESCs。以正常mESCs作为对照,在生长早期(第7-10代),Pogz−/− ESCs保持未分化。但在后期中缺失Pogz使(>15代)ESCs出现明显的细胞生长和增殖缺陷。细胞分裂标志物的IF染色和细胞凋亡分析进一步揭示POGZ既对细胞的正常有丝分裂进程至关重要,也是细胞存活或基因组稳定性所必需的。20代以后的Pogz−/− ESCs增殖困难且出现自分化、碱性磷酸酶AP活性降低、多能性基因表达降低和分化基因表达增加。正常细胞和早期突变型(第10代)的RNA-seq分析中,Pogz-/- ESCs中细胞衰老和凋亡有关的基因表达增加,减数分裂特异性同源重组基因失调。
随后,通过观察对照组和早期突变组的ESC形成的拟胚体(EB)形态和生殖层基因表达情况,以及分析对照组和突变组EB的RNA-seq数据,确认了POGZ与神经谱系基因的关联,并经由变异组和对照组形成的神经元结构,明确了在ESC神经诱导过程中,POGZ是神经祖基因表达上调的必要条件。
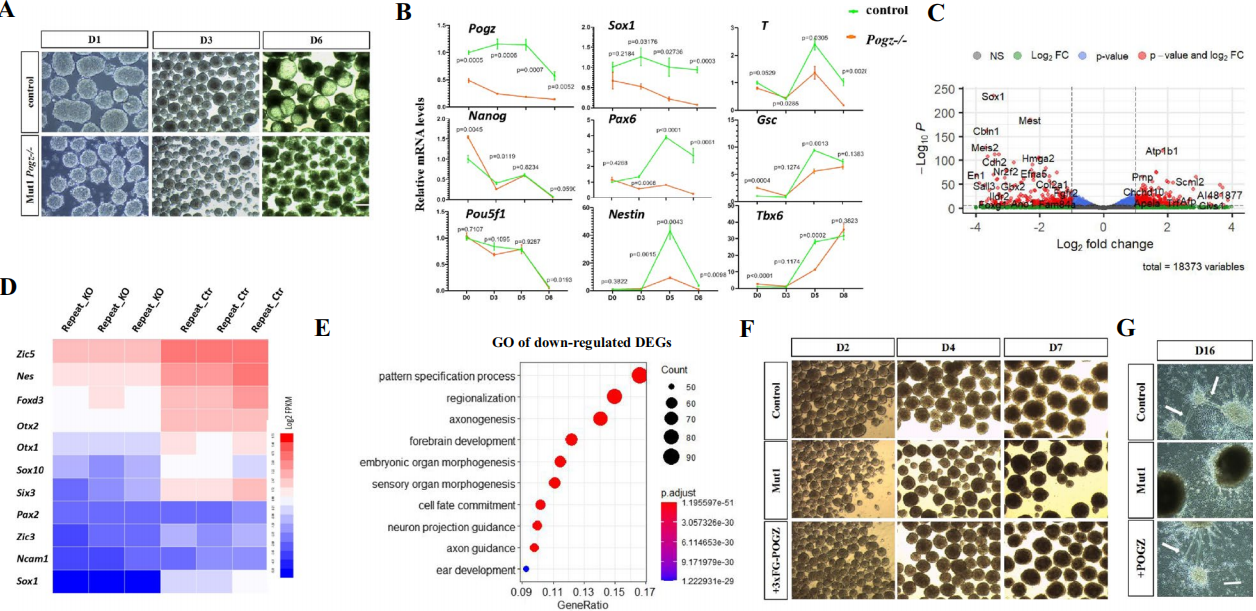
图2 POGZ缺失导致神经发育异常
2.POGZ和esBAF复合物结合
研究者利用IP结合质谱分析(IP-Mass Spec)发现POGZ与esBAF复合体密切相关,使用FLAG-POGZ Pogz-/- ESCs进行co-IP验证,以及利用双IF染色定位BRG1和POGZ,联合得出POGZ-Cter结构域介导其与BRG1的C-末端片段相互作用,从而与esBAF/BRG1复合物结合。
3.POGZ直接激活和抑制目标基因表达
为进一步了解POGZ的功能,研究者使用不同来源的商业POGZ抗体进行了ChIP-seq实验,但是效果不佳,因此选择使用FLAG-POGZ融合蛋白,在Pogz-/- ESCs中进行FLAG ChIP-seq和FLAG CUT&Tag实验。结果显示CUT&Tag的峰值强度比传统的ChIP-seq强很多。CUT&Tag识别到16728个明显富集的峰,主要定位于近端TSS和远端区域,并且POGZ占据的远端区域富集有静态增强子和活跃增强子。POGZ目标基因的KEGG功能富集主要是神经变性、帕金森和亨廷顿病通路。与RNA-seq数据联合分析,大约有538个与POGZ结合的基因在Pogz-/-ESCs中失调。342个上调的基因包括App(神经分化和轴突发生)、Mest和Impact,196个下调的基因包括多能性相关的基因(如Utf1和Lefty1)。因此POGZ既是转录激活因子又是抑制因子。
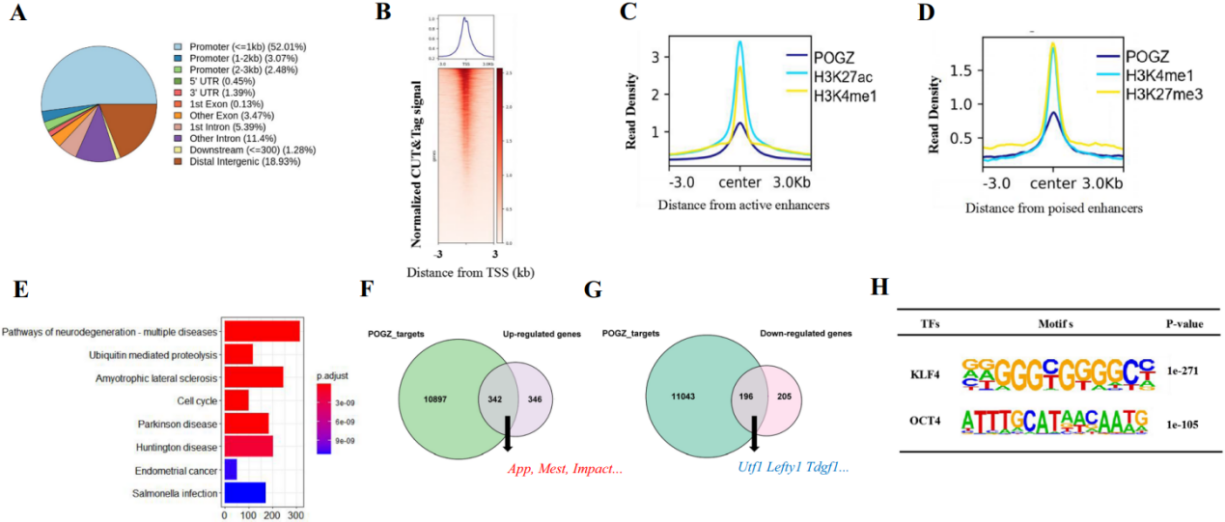
图3 POGZ主要定位于基因的启动子和增强子
随后使用HOMER对POGZ结合位点进行Motif分析, 显示POGZ与核心多能性因子NANOG/OCT4共享结合motif,并且全局荟萃分析显示POGZ类似于ESRRB、KLF4和Med1,信号富集在超级增强子上。双IF染色和co-IP证实POGZ与NANOG在ESCs的细胞核中明显共存且可以轻易地拉下内源性的OCT4。因此POGZ在维持ESCs干性方面起着重要作用。

图4 POGZ的功能与ESC命运相关
4.POGZ招募BRG1/esBAF至神经基因调节ESC神经诱导过程中的增强子活性
BRG1是esBAF的核心酶成分,它包括许多其他亚单位,如BAF155、BAF60a和SS18。POGZ CUT&Tag和BRG1 ChIP-seq显示两者的peak有广泛的重叠。对POGZ和BRG1结合位点的基因进行GO/KEGG功能分析,确认POGZ需要BRG1来调节与神经有关的过程。在Pogz-/- ESC衍生的神经球中,BRG1在神经祖细胞基因的启动子和增强子上的占有率降低。因此POGZ介导的BRG1招募对ESC的神经诱导非常重要。
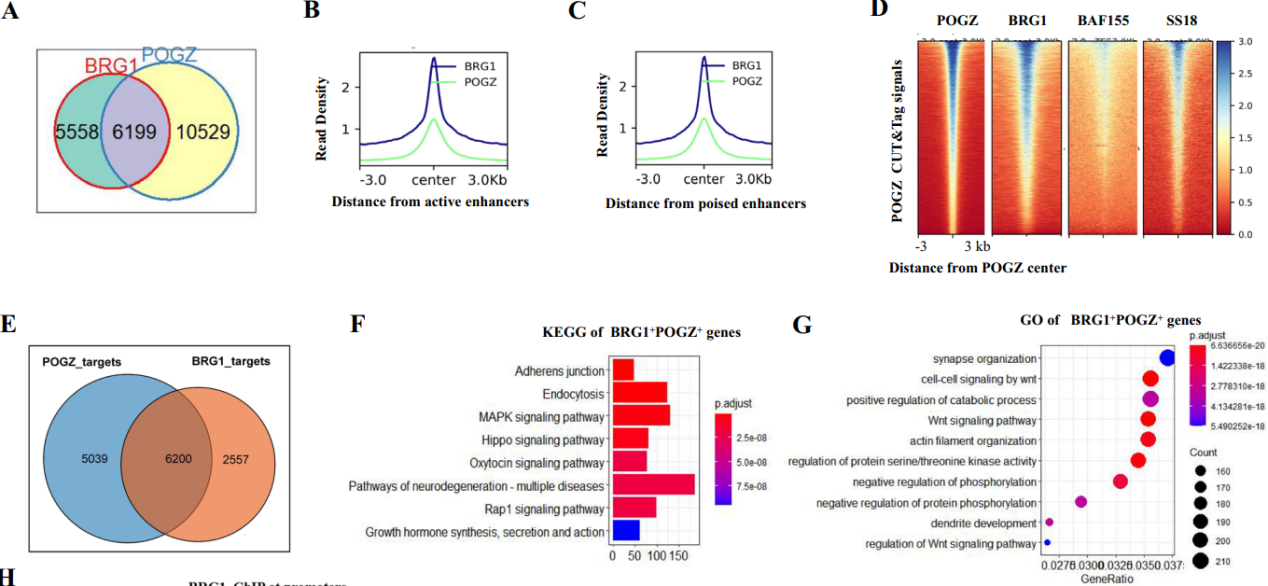
图5 POGZ将BRG1/esBAF招募到神经基因上
在对照组和早期传代的Pogz-/- ESC 进行ATAC-seq分析,发现后者POGZ结合位点的染色质开放性减小。联合H3K4me1和H3K27ac富集信号得知突变体ESC中活跃增强子和静息增强子的染色质可及性都有所下降,近端TSS区域则无变化,因此POGZ主要是通过使染色质更易接近来促进增强子活性。联合RNA-seq数据分析,表达上调且染色质开放性增加的基因富集于调节神经元分化和组织发育的通路。在缺失BRG1的ESC中,POGZ结合位点的染色质开放性减少。因此POGZ通过与BRG1结合促进染色质可及性。联合增强子和TSS处的H3K4me1/H3K27ac ChIP-seq信号,确认POGZ主要调节ESC的增强子活性。
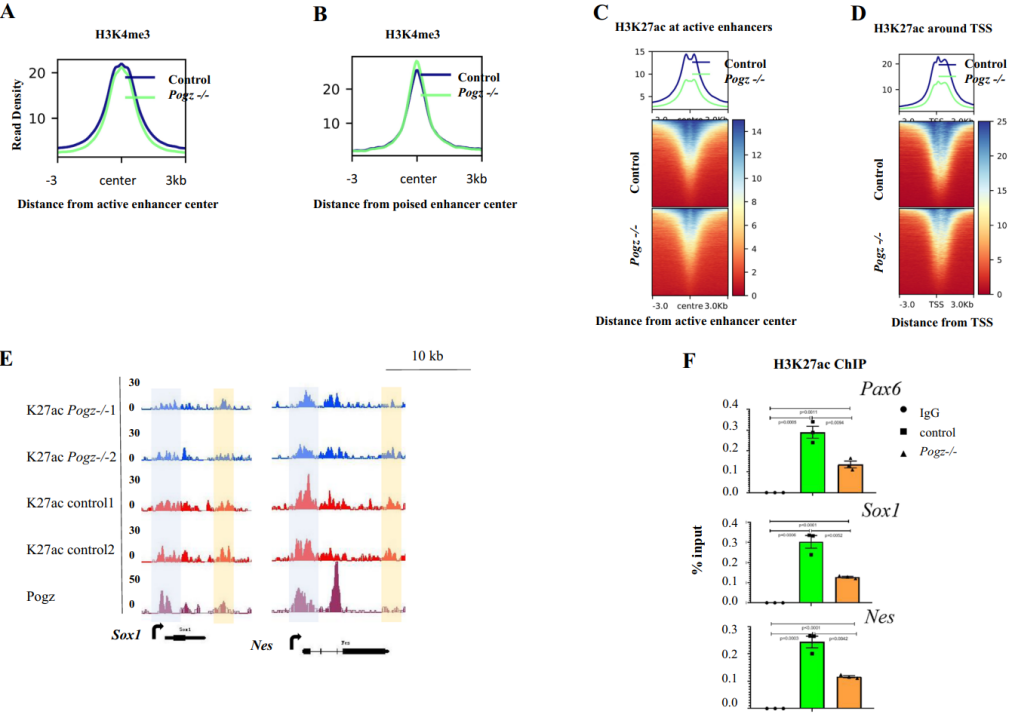
图6 POGZ调控ESC的增强子活性
综上所述,该研究提出POGZ既是一个转录因子又是一个染色质调控因子。POGZ的功能性丧失会导致基因表达异常和各种发育缺陷,特别是在神经发生期间的神经缺陷。作为转录因子,POGZ可以通过直接与关键调控元件结合来激活和抑制目标基因。作为重要的表观基因组调节因子,POGZ可以通过与esBAF染色质重塑复合物的结合来调节染色质状态。其中,FLAG-POGZ的CUT&Tag数据在该研究中起到了重要作用。
中科院水生所孙玉华研究员为该论文通讯作者,项目副研究员孙晓云和博士生程麟茜为论文的共同第一作者。该研究得到了国家重点研发项目的资助。
参考文献:
Sun X, Cheng L, Sun Y. Autism-associated protein POGZ controls ESCs and ESC neural induction by association with esBAF. Molecular Autism, 2022, 13(1): 1-18.
 微信公众号
微信公众号
