
1
R-loop的定义和特点
R-loop是一种由一条RNA单链侵入双链DNA,与其中一条DNA链结合,从而释放出一条DNA单链而形成的一种特殊的三链核酸结构。R-loop多在富含鸟嘌呤G(G-rich)的区域形成,该区域可被称为G簇。R-loop的形成起始后,DNA-RNA杂交链被延长,并通过随后的G-rich序列稳定下来。当鸟嘌呤G的含量降低,延长减少,R-loop的形成则停止[1-3]。
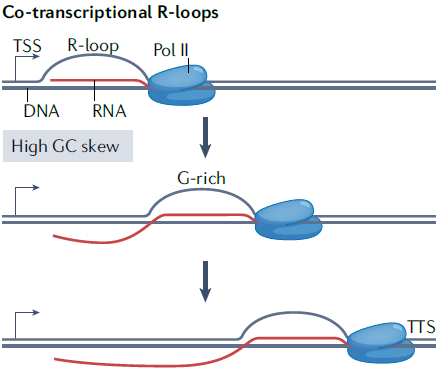
图1.转录过程中R-loop的形成
R-loop的形成与转录过程密不可分,所以其水平也受转录的调控,很多研究表明Pol II在DNA上的暂停(pausing)会诱导R-loop的产生。在分布方面,基因密度高的转录活跃的基因上通常可以检测到更多的R-loop;反之,基因密度较低的区域上R-loop则较少。一些拓扑异构酶、核酸酶、解旋酶、RNA加工因子以及核糖核酸酶RNase H1和RNase H2可以解除R-loop结构[1-3]。
2
R-loop对基因表达的影响
R-loop的功能具有两面性,细胞需要其带来的积极作用,也需要避免其异常产生带来的负面影响。具体而言,R-loop是很多重要生物学过程必需的中间产物,例如S区的R-loop是免疫球蛋白类开关重组过程的天然来源。CRISPR-Cas9系统中,由gRNA和双链DNA形成的R-loop直接引导Cas9核酸酶活性,产生DNA双链断裂。R-loop还可以在DNA损伤修复过程中充当关键中间体,但异常产生积累的R-loop又会给基因组带来不稳定性,其功能可谓是一把“双刃剑”[1-3]。

图2.R-loop功能的两面性
由于R-loop可能会驱动基因组的不稳定性,改变基因表达或细胞信号通路,因此其失调与许多人类疾病的发生发展有关,包括癌症、神经退行性变和自身免疫病等。在一些综合征、人类神经紊乱和癌症中都发现了大量的R-loop积累。以下表格中(篇幅有限,未截取全部)汇总了涉及R-loop的相关基因和关联的疾病名称[4]。
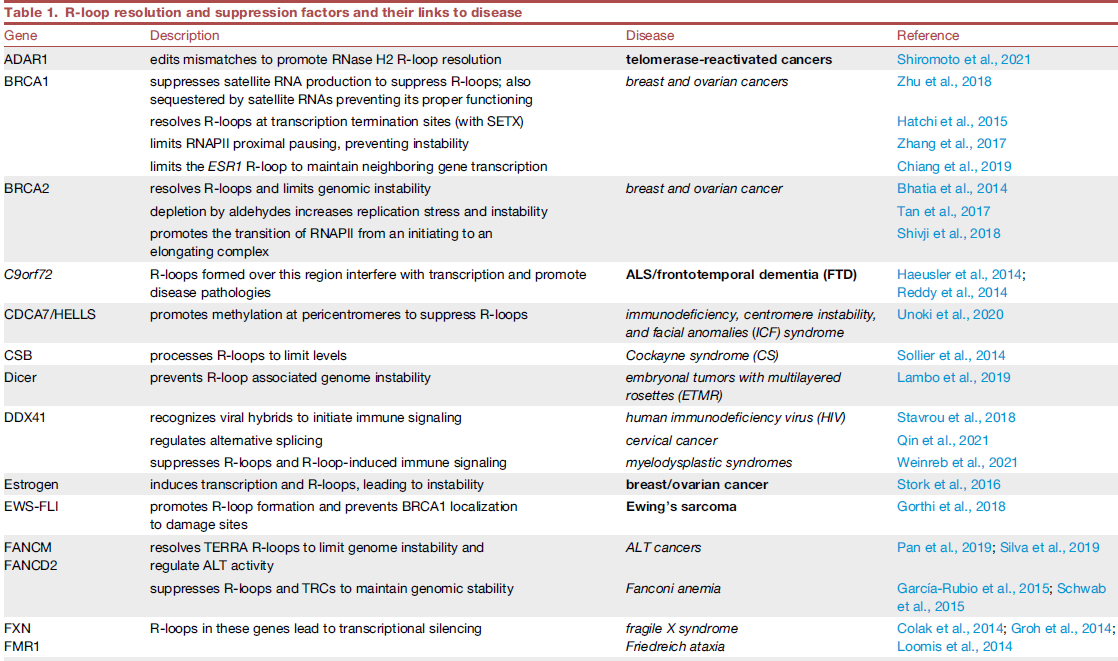
机制方面,有研究表明,启动子区的R-loop可以阻止DNA被甲基化和抑制因子的结合,从而起到促进转录的作用。而在转录终止区(polyA区),Pol II后的G-rich区域形成的R-loop可以招募人类解旋酶Senataxin 解除R-loop,进而使Xrn2蛋白利用其5’-3’核酸外切酶活性降解新生的RNA链,并将Pol II移出DNA链从而终止转录[5]。

图3.R-loop在启动子区促进转录
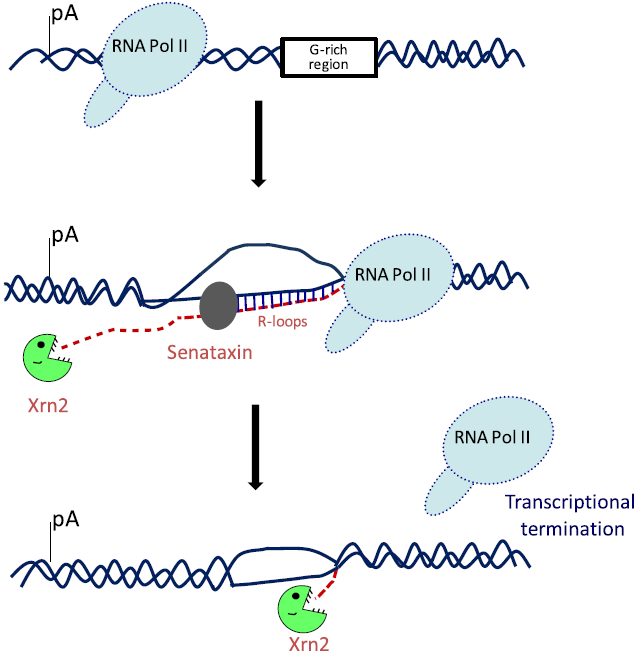
图4.R-loop在终止区终止转录
3
R-loop调控基因表达的文献案例
案例一
lncRNA HOTTIP形成的R-loop调节CTCF结合活性和TAD完整性 [6]
研究者以小鼠为模型,发现在急性髓系白血病(AML)发生过程中,一种lncRNA HOTTIP会异常激活,此lncRNA可以与部分CTCF结合位点附近的DNA形成R-loop。敲除HOTTIP后,CTNNB1(β-catenin)基因位点附近的CTCF结合(CBS)减少,此位点的R-loop减少,TAD边界强度减弱。
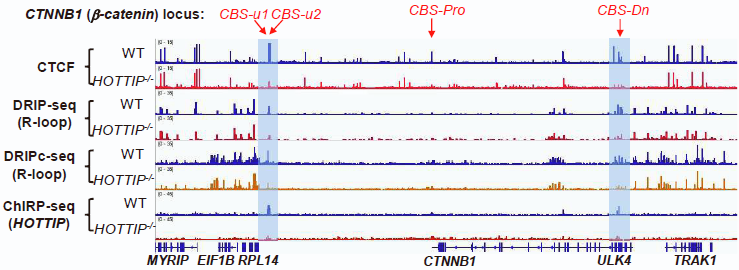
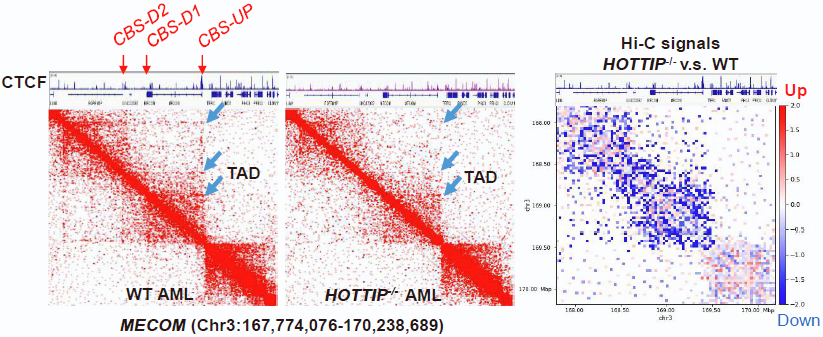
图5.敲除HOTTIP减少CTCF结合和减弱TAD边界强度
研究者经过一系列实验证实,提出了lncRNA HOTTIP的异常激活,通过对白血病相关的染色质重编程和改变基因转录,来影响造血干细胞,形成癌症的机制:HOTTIP通过与Wnt/β-catenin基因位点附近的CTCF结合位点形成R-loop,招募CTCF/cohesin结合到DNA,形成TAD边界,促使enhancer-promoter互作,激活癌基因表达,从而促进白血病发展。
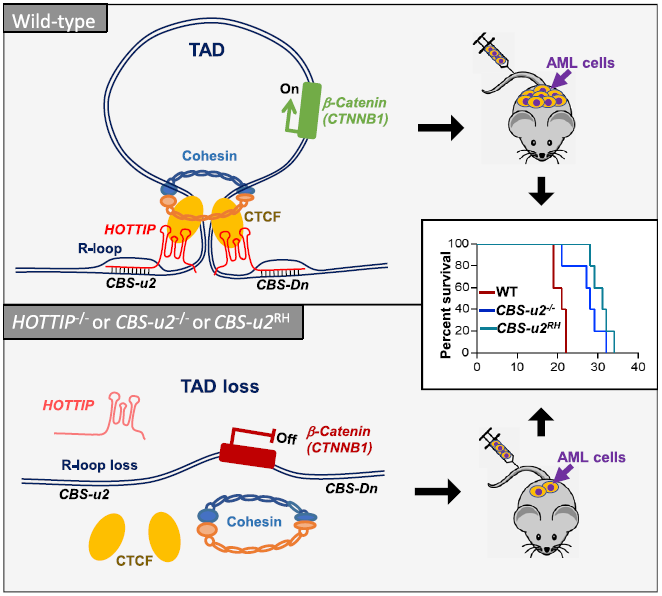
图6.lncRNA HOTTIP激活癌基因表达的机制
案例二
位点特异性R-loop诱导CGG重复收缩,重新激活脆性X基因FMR1 [7]
FMR1基因沉默会造成脆性X综合征(自闭症谱系障碍),此前有研究表明,FMR1基因中的CGG序列重复的扩张会影响CTCF结合,改变TAD边界的位置,引起FMR1基因表达沉默[8]。
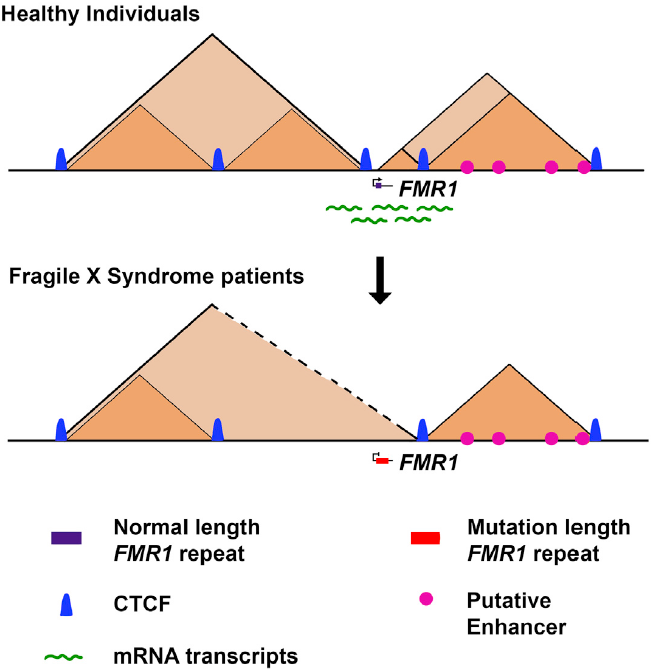
图7.FMR1基因序列重复扩张导致自身沉默的机制
那么如何在基因水平治疗此疾病呢?研究者发现通过导入一段靶向FMR1的CGG重复序列的RNA,可以在此位点特异性的形成R-loop,使此区域发生去甲基化并激活DNA修复途径,收缩CGG序列重复长度,从而重新激活/恢复FMR1基因的表达。
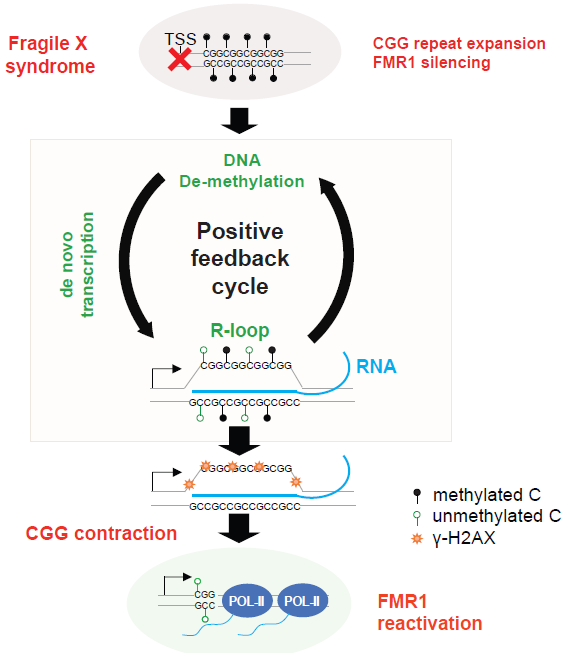
图8.位点特异性R-loop重新激活/恢复FMR1基因表达的机制
4
检测R-loop的技术方法
检测R-loop位点的实验方法可分为两大类:
一类是基于可特异性识别R-loop的抗体S9.6,代表性的技术是DRIP-seq,该方法的原理与ChIP-seq有些类似,由加州大学Frédéric Chédin团队首次开发,为了提高DRIP-seq的分辨率、特异性或敏感性,后来又出现了DRIPc-seq、bisDRIPseq和ssDRIP-seq等技术,其中ssDRIP-seq由清华大学孙前文老师的团队开发,可以获得链特异性DRIP-seq数据。
另一类是基于催化失活的RNase H1,此突变酶可特异性结合DNA-RNA杂合链但不行使RNA消化功能,然后再进行类似ChIP实验,代表性的技术是R-ChIP,由加州大学付向东老师团队开发(现已全职加入西湖大学)。

随着CUT&RUN和CUT&Tag逐步取代ChIP-seq之势,后续又有研究者利用MNase或Tn5酶代替ChIP过程对R-loop进行检测,分别开发出了MapR和R-loop CUT&Tag技术,其中R-loop CUT&Tag由武汉大学梁凯威/房萍萍课题组开发,因其简单高效,受到广泛关注。
在R-loop CUT&Tag实验中,可简单的使用S9.6抗体来识别R-loop,再使用pA/G-Tn5融合蛋白与抗体结合并特异性“切割”R-loop,回收DNA进行链置换后即可扩增完成文库构建,与现有的常规目标蛋白的 CUT&Tag差别不大,对于有CUT&Tag实验基础的研究者可以快速“上手”完成R-loop CUT&Tag建库[9]。
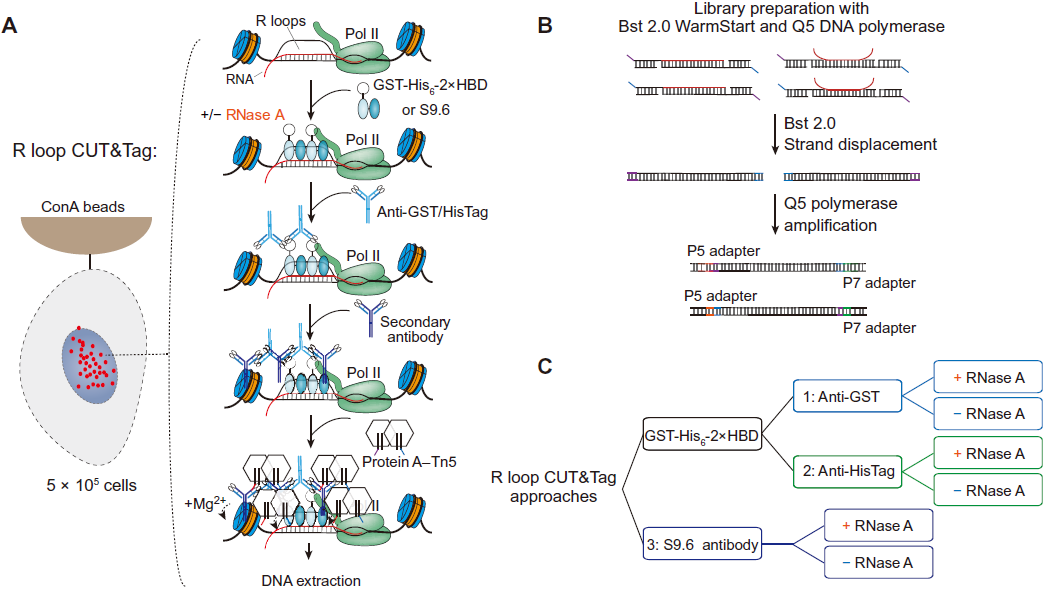
图9.R-loop CUT&Tag实验流程
与DRIP-seq技术相比,R-loop CUT&Tag、R-ChIP和MapR均在TSS处更加富集,而DRIP-seq技术则在gene body更富集,这可能是体内原位转座与体外免疫沉淀的策略不同所带来的结果差异,此外,DRIPc-seq的体外纯化和片段化过程可能会损坏一些R-loop结构。与R-ChIP和MapR相比,R-loop CUT&Tag则在检测gene body处R-loop的敏感性更高[9]。
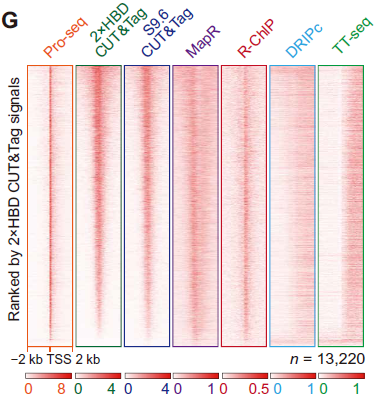
图10.R-loop相关检测技术在TSS上下游的信号分布
需注意的是,R-loop CUT&Tag实验需要平行构建1个阴性对照(RNase A或RNase H处理)文库,如下图所示,RNase H的处理并没有完全消除相应位点的R-loop信号,可能是因为一部分高GC的DNA-RNA杂交体对RNase H具有抗性[9]。
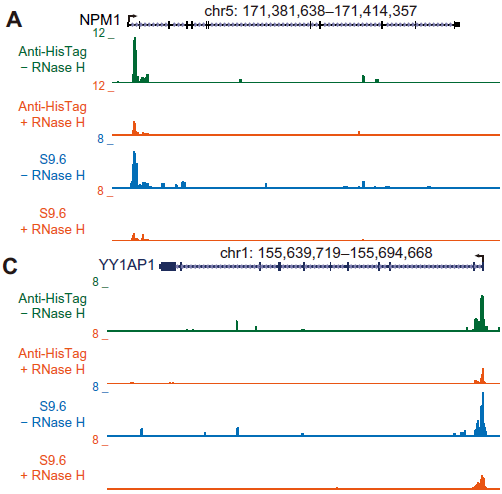
图11.R-loop CUT&Tag及阴性对照信号可视化
总 结
相比其它技术,基于S9.6抗体的R-loop CUT&Tag更简单高效,它无需交联、超声、限制性酶切、转基因细胞系构建等复杂步骤,最快仅需1天时间,细胞量要求更少,数据结果富集好,背景低,还更灵敏,适用于对R-loop感兴趣的广大研究者快速高效的获得细胞内R-loop分布位点,助力解析和进一步丰富基因表达的表观调控机制。

参考文献:
[1]张译匀,叶素敏,金建平. R-loop的调控及其生理功能。生物化学与生物物理进展,2023.
[2]Youssef, et al. The balancing act of R-loop biology: The good, the bad, and the ugly. 2020, Journal of Biological Chemistry.
[3]Petermann, et al. Sources, resolution and physiological relevance of R-loops and RNA–DNA hybrids. 2020, Nature Reviews Molecular Cell Biology.
[4]Brickner, et al. Walking a tightrope: The complex balancing act of R-loops in genome stability. 2022, Molecular Cell.
[5]Konstantina, et al. Human Senataxin Resolves RNA/DNA Hybrids Formed at Transcriptional Pause Sites to Promote Xrn2-Dependent Termination. 2011, Molecular Cell.
[6]Luo, et al. HOTTIP-dependent R-loop formation regulates CTCF boundary activity and TAD integrity in leukemia. 2022, Molecular Cell.
[7]Lee, et al. Site-specific R-loops induce CGG repeat contraction and fragile X gene reactivation. 2023, Cell.
[8]Sun, et al. Disease-Associated Short Tandem Repeats Co-localize with Chromatin Domain Boundaries. 2018, Cell.
[9]Wang, et al. Genomic profiling of native R loops with a DNA-RNA hybrid recognition sensor. 2021, Science Advances.
 微信公众号
微信公众号
